
����Ŀ����.50mL0.5mol��L-1��������50mL0.55mol��L-1��NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ�����зų��������ɼ����к��ȡ��ش��������⣺

(1)��ʵ��װ���Ͽ�����֪��ͼװ������������֮������ָ��____________________
(2)�ڲⶨ�к��ȵ�ʵ���У����㷴Ӧ��ʱ��Ҫ��������________________
�����Ũ�Ⱥ���� �ڼ��Ũ�Ⱥ���� �۱�����
�ܷ�Ӧǰ����Һ���¶Ȳ� �ݲ�������ʱ��
A.�٢ڢۢ� B. �٢ڢۢ� C. �ڢۢܢ� D. �٢ۢܢ�
(3)ʵ���и���60mL0.50mol��L-1�������50mL0.55mol��L-1��NaOH��Һ���з�Ӧ��������ʵ����ȣ������к���_______ (���ȡ�����ȡ�)�����ų�������____ (���ȡ�����ȡ�)
(4)����ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ��������ʵ�飬��õ��к�����ֵ��_____���ƫ����ƫС������Ӱ�족����
��.�״�����Ҫ�Ĺ�ҵԭ�ϡ�ú������������ú̿��ȡˮú���Ӷ��ϳɼ״���CO(g)+2H2(g)![]() CH3OH(g)����֪������ͼΪ��Ӧ�������仯�����ʼ���
CH3OH(g)����֪������ͼΪ��Ӧ�������仯�����ʼ���


��CO(g)��1/2O2(g)===CO2(g) ��H=��280kJ/mol
H2(g)��1/2O2(g)===H2O(l) ��H=��284kJ/mol
H2O(l)===H2O(g) ��H=+ 44kJ/mol
��ش��������⣺
(1)��д����ʾ��̬�״�ȼ���ȵ��Ȼ�ѧ����ʽ_________________________��
(2)H��O���ļ���xΪ_________kJ/mol��
(3)�״�����ֽ�ΪCO��H2��������ķ�Ӧ�Ļ��Ϊ_________kJ/mol��
���𰸡� ���β�����������ڴ�С�ձ���û������ֽ��
����С�ձ��ڲ���ƽ B ��� ����� ƫС CH3OH(g)+ ![]() O2(g)=CO2(g)+2H2O(l)��H=-757kJmol-1 462 510
O2(g)=CO2(g)+2H2O(l)��H=-757kJmol-1 462 510
����������. (1)װ��ͼ�д�����û��ʹ�����β�����������ڴ�С�ձ���û������ֽ������С�ձ��ڲ���ƽ��
(2)���ݷ�Ӧ�ȵļ��㹫ʽ��H=Q=-cm��T��֪����Ӧ���к��ȼ���ʱ��������Ҫ�������У�������c����Ӧ����Һ�������Լ�����ˮ�����ʵ���m����Ӧǰ���¶ȣ����ݷ�Ӧǰ����¶Ȼ�÷�Ӧǰ���¶ȱ仯��T������Ҫ���ݢ٢ڢۢܣ��ʴ�ΪB��
(3)�к��ȵľ���ǿ���ǿ�Ӧ����1molˮʱ�ų����ȣ������������أ�������60mL0.50molL-1������Һ��������ʵ�飬����к�����ֵ��ȣ�����Ӧ�ų����������������Լ�������Ķ����йأ�������60mL0.5molL-1������Һ��50mL0.55molL-1NaOH��Һ���з�Ӧ��������ʵ����ȣ�����ˮ�������࣬���ų�������ƫ�ߣ������ηų�����������ȡ�
(4)NH3H2O��������ʣ��������Ϊ���ȹ��̣������ð�ˮ����ϡ����������Һ��Ӧ����Ӧ�ų�������С��57.3kJ������õ��к�����ֵ��ƫС��
��.(1)ȼ���ȵ��Ȼ�ѧ����ʽ�У���ȼ��Ϊ1mol����Ӧ�����ȶ��������
��ͼ1�ɵ��Ȼ�ѧ����ʽ����CO��g��+2H2��l��=CH3OH��g����H=-91kJ/mol��
����֪����CO��g��+![]() O2��g���TCO2��g����H=-280kJ/mol����H2��g��+
O2��g���TCO2��g����H=-280kJ/mol����H2��g��+![]() O2��g���TH2O��l����H=-284 kJ/mol�����ݸ�˹���ɣ�����2+��-�ٿɵã�CH3OH��g��+
O2��g���TH2O��l����H=-284 kJ/mol�����ݸ�˹���ɣ�����2+��-�ٿɵã�CH3OH��g��+![]() O2��g��=CO2��g��+2H2O��l����H=-757kJmol-1��
O2��g��=CO2��g��+2H2O��l����H=-757kJmol-1��
(2)��֪��H2��g��+![]() O2��g���TH2O��l����H=-284 kJ/mol��H2O��l���TH2O��g����H=+44kJ/mol��������ӿɵã�H2��g��+
O2��g���TH2O��l����H=-284 kJ/mol��H2O��l���TH2O��g����H=+44kJ/mol��������ӿɵã�H2��g��+![]() O2��g���TH2O��g����H=-240 kJ/mol����Ӧ��=��Ӧ���ܼ���-�������ܼ��ܣ���436kJ/mol+
O2��g���TH2O��g����H=-240 kJ/mol����Ӧ��=��Ӧ���ܼ���-�������ܼ��ܣ���436kJ/mol+![]() ��496kJ/mol-2��x kJ/mol=-240kJ/mol�����x=462��
��496kJ/mol-2��x kJ/mol=-240kJ/mol�����x=462��
(3)��ͼ�ο�֪�״��Ļ��Ϊ��419+91��kJ/mol=510kJ/mol��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�� úȼ���ŷŵ���������SO2��NOx���γ����ꡢ��Ⱦ����������NaClO2��Һ��Ϊ���ռ���ͬʱ���������������������ش��������⣺
��1��NaClO2�Ļ�ѧ����Ϊ_______��
��2���ڹ��ݷ�Ӧ����ͨ�뺬��SO2��NO����������Ӧ�¶�Ϊ323 K��NaClO2��ҺŨ��Ϊ5��103 mol��L1 ����Ӧһ��ʱ�����Һ������Ũ�ȵķ���������±���
���� | SO42 | SO32 | NO3 | NO2 | Cl |
c/��mol��L1�� | 8.35��104 | 6.87��106 | 1.5��104 | 1.2��105 | 3.4��103 |
��д��NaClO2��Һ������������Ҫ��Ӧ�����ӷ���ʽ__________������ѹǿ��NO��ת����______�����ߡ��������䡱���͡�����
���������շ�Ӧ�Ľ��У����ռ���Һ��pH��______ ����������䡱��С������
����ʵ������֪������Ӧ����______������Ӧ���ʣ�����ڡ���С�ڡ�����ԭ���dz���SO2��NO�������еij�ʼŨ�Ȳ�ͬ����������___________��
��3���ڲ�ͬ�¶��£�NaClO2��Һ���������ķ�Ӧ�У�SO2��NO��ƽ���ѹpe��ͼ��ʾ��

����ͼ������֪����Ӧ�¶����ߣ�����������Ӧ��ƽ�ⳣ����______________������������䡱��С������
�ڷ�ӦClO2+2SO32===2SO42+Cl��ƽ�ⳣ��K����ʽΪ___________��
��4���������NaClO��Ca��ClO��2���NaClO2��Ҳ�ܵõ��Ϻõ���������Ч����
�ٴӻ�ѧƽ��ԭ��������Ca��ClO��2���NaClO���е��ŵ���_______��
����֪���з�Ӧ��
SO2(g)+2OH (aq) ===SO32 (aq)+H2O(l) ��H1
ClO (aq)+SO32 (aq) ===SO42 (aq)+Cl (aq) ��H2
CaSO4(s) ===Ca2+��aq��+SO42��aq�� ��H3
��ӦSO2(g)+ Ca2+��aq��+ ClO (aq) +2OH (aq) === CaSO4(s) +H2O(l) +Cl (aq)�Ħ�H=______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�̶��ݻ����ܱ������н������·�Ӧ��CO2(g)+H2(g)CO(g)+H2O(g)����ƽ�ⳣ��K���¶�t�Ĺ�ϵ���£�
T/�� | 700 | 800 | 850 | 1000 | 1200 |
K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(1)K�ı���ʽΪ�� .
(2)�÷�Ӧ������ӦΪ ��Ӧ(�����ȡ����ȡ�).
(3)���жϸ÷�Ӧ�Ƿ��Ѿ��ﵽ��ѧƽ��״̬���� .
A��������ѹǿ����
B�����������COŨ�Ȳ���
C��v��(H2)=v��(H2O)
D��c(CO2)=C(CO)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����װ����ͼ��ʾ��

��.���ö��Ե缫���ʱ��cΪ____________�����缫��Ӧ________dΪ____________��,�缫��Ӧ______________������ܷ�Ӧ�Ļ�ѧ����____________________
��.(1)���ô�װ�ý������϶�ͭ��cΪ__________��������ͭ��dΪ___________��������ͭ�����ҺŨ��_____________(����С�䣩
(2�����һ��ʱ���Ե缫���г�����������������Ϊ16�ˣ����·��ת�Ƶĵ���___________mol.
��.���ô�װ�ý��д�ͭ�ĵ�⾫������Ҫ���ͭ����ͼ�е缫________(��ͼ�е���ĸ)������ͭ�л�����Au��Ag��Fe����Fe��_______(�����ӷ��ţ���ʽ������Һ��c�缫�����ķ�Ӧ______________��________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˱������������������Դ��ij�о�С��ͨ�����¼����̣�����ҵ�����������������������Ҫ��Fe2O3���ڣ�ת�����Ҫ�Ļ���ԭ��FeSO4����Ӧ�����ԣ���
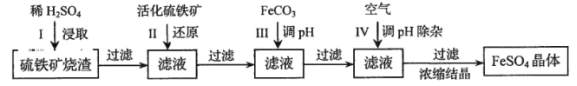
�������ԭFe3+����Ҫ��ӦΪ��FeS2+7Fe2(SO4)3+8H2O=15FeSO4+8H2SO4��������������Ӧ����ش��������⣺
��1���ڢ�H2SO4��Fe2O3��Ӧ�����ӷ���ʽ�� ��
��2������ڢ���Fe3+�Ƿ���ȫ��ԭ��Ӧѡ�� ������ĸ��ţ���
A��KMnO4��Һ B��K3[Fe(CN)6]��Һ C��KSCN��Һ
��3���ڢ�FeCO3����ҺpH��5.8���ң�Ȼ���ڵڢ���ͨ�����ʹ��ҺpH����5.2����ʱFe2+����������Һ�����������ʳ�����ͨ�����������ҺpH���͵�ԭ���� ��
��4��FeSO4��ת��ΪFeCO3��FeCO3�ڿ����м��ȷ�Ӧ���Ƶ���ϵ��������ϡ�
��֪25�棬101kPaʱ��4Fe(s) + 3O2 (g) =2Fe2O3(s) ![]() =-1648kJ/mol
=-1648kJ/mol
C(s)+O2(g)=CO2(g) ![]() =-393kJ/mol
=-393kJ/mol
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s) ![]() =-1480kJ/mol
=-1480kJ/mol
FeCO3�ڿ����м��ȷ�Ӧ����Fe2O3���Ȼ�ѧ����ʽ�� ��
��5��FeSO4��һ�������¿��Ƶ�FeS2(��������)���ײ��ϡ��ò��Ͽ��������������﮵�أ���طŵ�ʱ���ܷ�ӦΪ4Li+ FeS2= Fe +2Li2S��������Ӧʽ�� ��
��6�����������е���ȫ����ΪFe2O3���京��Ϊ50%����a kg��������Ϊb%��������뵽c kg�����н�ȡ�����Ľ�ȡ��Ϊ96%���������ʽ������ĵ������Լ���pH����Һ��������������������Բ��ơ����������̣��ڢ�Ӧ����FeCO3 kg��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Ӧ����1��Cu+2Fe3+=Cu2++2Fe2+��2��Fe+Cu2+=Fe2++Cu���ж�Fe3+��Fe2+��Cu2+������ǿ��˳��������ȷ����
A. Fe3+>Cu2+>Fe2+
B. Cu2+>Fe3+>Fe2+
C. Fe3+Fe2+>Cu2+
D. Fe2+>Cu2+>Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���3 mol CO2��2 mol H2�����2 L���ܱ������У��������·�Ӧ��
CO2(g)��H2(g)![]() CO(g)��H2O(g)��
CO(g)��H2O(g)��
(1)�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK��________��
(2)��֪��700 ��ʱ���÷�Ӧ��ƽ�ⳣ��K1��0.5������¶��·�ӦCO(g)��H2O(g)![]() CO2(g)��H2(g)��ƽ�ⳣ��K2��________
CO2(g)��H2(g)��ƽ�ⳣ��K2��________
(3)��֪��1000 ��ʱ���÷�Ӧ��ƽ�ⳣ��K3��1.0����÷�ӦΪ_________��Ӧ(����ȡ����ȡ�)��
(4)��1 000 ���£��ӿ�ʼ��20sʱ��Ӧ�ﵽƽ��״̬����COŨ��Ϊ____________mol/L��CO2��ת����Ϊ____________�����¶��£���ijʱ��CO2�����ʵ���Ϊ2 mol�����ʱv��______________v��(�>������������<��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾװ�ý�������ʵ�飺��������Һ������У�Ԥ���������ʵ��������ǣ� ��

ѡ�� | �������� | �������� | Ԥ����е����� |
A�� | ϡ���� | ̼�������������ƵĻ����Һ | ������������ |
B�� | Ũ���� | ��ɰֽ��ĥ�������� | ��������ɫ���� |
C�� | �Ȼ�����Һ | Ũ����������Һ | ����������ɫ���� |
D�� | ������Һ | �������������Һ | ��Һ����ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A��ԭ��ص��������ϱ����ǽ���
B��ԭ��صĸ���������ԭ��Ӧ
C��ʵ������������ȡ�����������ô�п��ϡ���ᷴӦ
D��ԭ��ؿ��������ڲ�������ȫ��ת��Ϊ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com