
 2NH3(g) ΔH=-92 kJ·mol-1。请回答下列问题:
2NH3(g) ΔH=-92 kJ·mol-1。请回答下列问题:
 0.1 mol CuO 8g
0.1 mol CuO 8g


科目:高中化学 来源:不详 题型:填空题
 CO2(g)+H2(g),得到如下二组数据:
CO2(g)+H2(g),得到如下二组数据:| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在分子中,两个成键的原子间的距离叫做键长 |
| B.H—Cl的键能为431.8 kJ/mol,H—I的键能为298.7 kJ/mol,这可以说明HCl分子比HI分子稳定 |
| C.含有极性键的分子一定是极性分子 |
| D.键能越大,表示该分子越容易受热分解 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.已知:HCl和NaOH反应的中和热:ΔH=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的 中和热ΔH=2×(-57.3)kJ/mol |
| B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)= 2CO(g)+O2(g)反应的ΔH=2×(+283.0)kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
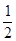 H2SO4(l)+NaOH(l)=
H2SO4(l)+NaOH(l)= 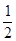 Na2SO4(l)+ H2O(l);△H=-57.3KJ/mol
Na2SO4(l)+ H2O(l);△H=-57.3KJ/mol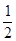 O2(g)= CO2(g);△H=-283KJ/mol
O2(g)= CO2(g);△H=-283KJ/mol查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 O2(g)=CO2(g) △H=-283.0kJ·mol—1
O2(g)=CO2(g) △H=-283.0kJ·mol—1 S(g)+2CO2(g),CO2的物质的量分数随时间的变化如图所示,则:
S(g)+2CO2(g),CO2的物质的量分数随时间的变化如图所示,则: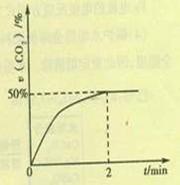
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯化铝和干冰升华 | B.钠和硫熔化 |
| C.食盐和氯化氢溶解于水 | D.二氧化硅和二氧化硫熔化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com