
| A、pH=1的溶液中:Na+、Fe2+、NO3-、SO42- |
| B、c(OH-)=10-12的溶液中:NH4+、Al3+、NO3-、Cl- |
| C、由水电离的c(H+)=1×10-13mol?L-1的溶液中:Ba2+、K+、Cl-、[Al(OH)4]- |
| D、能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO32- |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

| A、在任何溶液中,c(Ca2+)、c(SO42-)均相等 |
| B、d点溶液通过蒸发可以变到c点 |
| C、a点对应的Ksp等于c点对应的Ksp |
| D、b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×10-3mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知常温下HF的Ka=3.6×10-4;CH3COOH的Ka=1.8×10-5.现有①0.2mol/L KOH溶液、②0.2mol/L CH3COOH溶液、③0.2mol/L HF溶液、④0.2mol/L HCl溶液,则:
已知常温下HF的Ka=3.6×10-4;CH3COOH的Ka=1.8×10-5.现有①0.2mol/L KOH溶液、②0.2mol/L CH3COOH溶液、③0.2mol/L HF溶液、④0.2mol/L HCl溶液,则:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeCl3溶液与Cu反应:Fe3++Cu═Fe2++Cu2+ |
| B、硫酸溶液与氢氧化钡溶液混合:SO42-+Ba2+═BaSO4↓ |
| C、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-=Mn2++Cl2+2H2O |
| D、Cu溶于足量浓硝酸:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合溶液中由水电离出的c(H+)=1×10-5mol/L | ||||
| B、c(A-)+c(HA)=2c(Na+)=0.4mol/L | ||||
C、HA溶液中
| ||||
| D、c(A-)-c(HA)=2c(OH-)-2c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
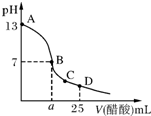
 常温下将HA和HB两种一元酸的溶液分别加水稀释,稀释时溶液pH的变化如图所示.以下叙述中不正确的是.( )
常温下将HA和HB两种一元酸的溶液分别加水稀释,稀释时溶液pH的变化如图所示.以下叙述中不正确的是.( )| A、HB是一种弱酸 |
| B、稀释前,c(HA)<10c(HB) |
| C、在NaB和HB的混合溶液中一定存在:c(B-)>c(Na+)>c(H+)>c(OH-) |
| D、在M点的两种溶液中:c(B-)=c(A-),且c(B-)+c(H+)>c(A-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
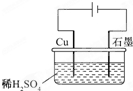
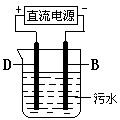
| A、电解过程中,铜电极上有H2产生 | ||||
B、电解初期,主反应方程式为:Cu+H2SO4
| ||||
| C、电解一定时间后,石墨电极上有铜析出 | ||||
| D、整个电解过程中,H+的浓度不断增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com