
| A. | FeCl3溶液和CuCl2溶液 | B. | Na2SO4溶液和NaCl溶液 | ||
| C. | AlCl3溶液和NaOH溶液 | D. | 盐酸溶液和Na2CO3溶液 |
分析 先观察试剂的颜色,如只用试管和胶头滴管而不用其它试剂就能区分,说明反应现象与反应物的量有关,且滴加顺序不同,反应现象不同,结合物质间的反应来分析解答.
解答 解:A.黄色为FeCl3溶液,蓝色为CuCl2溶液,故A不选;
B.二者不反应,均为无色溶液,不能鉴别,故B选;
C.NaOH少量反应生成沉淀,NaOH过量无沉淀生成,可鉴别,故C不选;
D.当盐酸少量时,离子反应方程式为CO32-+H+=HCO3-,当盐酸过量时,离子反应方程式为2H++CO32-=CO2↑+H2O,所以反应现象不同,可鉴别,故D不选;
故选B.
点评 本题考查物质的鉴别,为高频考点,把握试剂的颜色、与量有关的化学反应为解答关键为解答该题的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
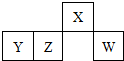 下表为元素周期表的一部分,X、Y、Z、W均为短周期元素,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )
下表为元素周期表的一部分,X、Y、Z、W均为短周期元素,其中W原子的最外层电子数是最内层电子数的3倍.下列判断正确的是( )| A. | 最高价氧化物对应水化物的酸性Y>Z>W | |
| B. | WO2可使酸性高锰酸钾褪色,说明WO2有漂白性 | |
| C. | ZCl4电子式: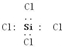 | |
| D. | X的气态氢化物可与W的最高价氧化物对应水化物相互反应生成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ABC | B. | CBA | C. | BCA | D. | BAC |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
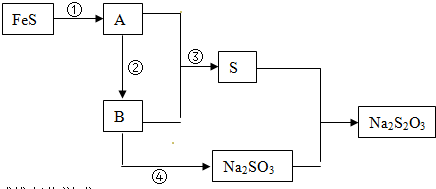
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N元素的电负性较大,但N2的化学性质很稳定 | |
| B. | 稀有气体一般难发生反应 | |
| C. | HF、HCl、HBr、HI的稳定性逐渐减弱 | |
| D. | F2比O2更容易与H2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
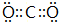 ,E的电子式
,E的电子式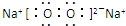 ,其中E含有非极性共价键(填“离子键”、“极性共价键”或“非极性共价键”)
,其中E含有非极性共价键(填“离子键”、“极性共价键”或“非极性共价键”)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第2周期元素氢化物的稳定性顺序是HF>H2O>NH3;则第3周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 | |
| B. | ⅣA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则ⅤA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 | |
| C. | 晶体中有阴离子,必有阳离子;则晶体中有阳离子,必有阴离子 | |
| D. | I-I键的键能比F-F、Cl-Cl、Br-Br键的键能都小;则在卤素单质中碘的熔点最低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 降低了反应的活化能 | B. | 增大了反应物、生成物的能量 | ||
| C. | 降低了反应的焓变 | D. | 增大了反应的平衡常数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com