
【题目】下列说法中,正确的是 ( )。
A. 煤是由有机化合物和无机化合物组成的复杂的混合物
B. 煤是结构复杂的含碳化合物
C. 煤的干馏和木材的干馏发生的都是化学变化,而且干馏产物也相同
D. 煤含有苯和甲苯,可先用干馏,后分馏的方法将它们分离出来
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】能在水溶液中大量共存的一组离子是
A.H+、I-、NO3-、CO32-B.NH4+、Fe3+、OH-、Br-
C.K+、Cl-、Cu2+、NO3-D.Al3+、SO42-、Na+、S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiH(氢化锂)常用作干燥剂、氢气发生剂等,可利用下列反应制备:2Li(熔融)+H2 ![]() 2LiH.有关说法不正确的是( )
2LiH.有关说法不正确的是( )
A.微粒半径:r(H﹣)>r(H+)
B.H﹣与Li+电子层结构相同
C.还原性:H>Li
D.碱性:LiOH<NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列化合物:①硝基苯 ②环己烷 ③乙苯 ④溴苯 ⑤间二硝基苯.其中能由苯通过一步反应直接制取的是( )
A. ①②③ B. ①③⑤ C. ①②④ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【贵州省遵义航天高级中学2017届高三第十一次模拟(5月)理科综合化学试题】 图1为光伏并网发电装置示意图。图2为电解尿素[CO(NH2)2]的碱性溶液制氢装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。

图1 光伏并网发电装置 图2 电解尿素的碱性溶液制氢装置
下列叙述中正确的是( )
A. 图1中N型半导体为正极,P型半导体为负极
B. 图2溶液中电子从B极流向A极
C. X2为氧气
D. 工作时,A极的电极反应式为CO(NH2)2 + 8OH- - 6e- = CO32- + N2↑+ 6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. H2SO4 的摩尔质量为98 B. 1 mol H2SO4 的质量是98g/mol
C. 0.5mol的氧 D. 6.02×1022个 H2SO4 分子的质量为9.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中要配制0.2 mol/L的NaCl溶液450 mL,配制时选用的容量瓶的规格和应称取的NaCl分别是 ( )
A. 450 mL、5.27 g B. 500 mL、5.85 g C. 450 mL、5.85 g D. 500 mL、5.27 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五氯化磷(PCl5)是有机合成中重要的氯化剂,可以由三氯化磷(PCl3)氯化得到:
PCl3(g)+Cl2(g)![]() PCl5(g) ΔH=-93.0 kJ·mol-1。某温度下,在容积恒定为2.0 L的密闭容器中充入2.0 mol PCl3和1.0 mol Cl2,一段时间后反应达平衡状态,实验数据如下表所示:
PCl5(g) ΔH=-93.0 kJ·mol-1。某温度下,在容积恒定为2.0 L的密闭容器中充入2.0 mol PCl3和1.0 mol Cl2,一段时间后反应达平衡状态,实验数据如下表所示:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl5)/mol | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(1)0~150 s内的平均反应速率v(PCl3)=________mol·L-1·s-1。
(2)该温度下,此反应的化学平衡常数的数值为____(可用分数表示)。
(3)反应至250 s时,该反应放出的热量为________kJ。
(4)下列关于上述反应的说法中,正确的是______(填字母)。
a.无论是否达平衡状态,混合气体的密度始终不变
b.300 s时,升高温度,正、逆反应速率同时增大
c.350 s时,向该密闭容器中充入氮气,平衡向正反应方向移动
d.相同条件下,若起始向该密闭容器中充入1.0 mol PCl3和0.2 mol Cl2,达到化学平衡状态时,n(PCl5)<0.20 mol
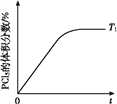
(5)温度T1时,混合气体中PCl5的体积分数随时间t变化的示意图如上。其他条件相同,请在上图中画出温度为T2(T2>T1)时,PCl5的体积分数随时间变化的曲线________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化物的叙述正确的是()
A. 酸性氧化物均可跟碱反应 B. 酸性氧化物在常温常压下均为气态
C. 金属氧化物都是碱性氧化物 D. 不能跟酸反应的氧化物一定能跟碱反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com