
 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源:不详 题型:填空题
 CO2(g)+H2(g) △H<0试回答下列问题:
CO2(g)+H2(g) △H<0试回答下列问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1,c(B)="0.200" mol·L-1,c(C)="0" mol·L-1。反应物A的浓度随时间的变化如右图所示。下列说法正确的是 ( )
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol·L-1,c(B)="0.200" mol·L-1,c(C)="0" mol·L-1。反应物A的浓度随时间的变化如右图所示。下列说法正确的是 ( )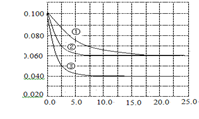
 C的△H>0
C的△H>0查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H+(aq) + In-(aq)
H+(aq) + In-(aq)| A.①④ | B.②⑤⑥ | C.①④⑤ | D.②③⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,测
zC(g),平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,测| A.x+y<z | B.平衡正向移动 | C.A的转化率降低 | D.C的体积分数增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CH3OH(g) △H<0,各物质的浓度如下表
CH3OH(g) △H<0,各物质的浓度如下表
| A.2min-4min内用氢气表示的速率为0.3mol/(L?min) |
| B.达平衡时,CO的转化率为62.5% |
| C.反应在第2min时改变了条件,可能是加入了催化刺 |
| D.反应在第2min时改变了条件,可能增加了H2的浓度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OCH3(g)+CO2(g) △H< 0。一定条件下得密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是 (填字母代号)。
CH3OCH3(g)+CO2(g) △H< 0。一定条件下得密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是 (填字母代号)。| A.高温高压 | B.加入催化剂 |
| C.减少CO2的浓度 | D.增加CO的浓度 E.分离出二甲醚 |
 CH3OCH3(g)+H2O(g),某温度下得平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g),某温度下得平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol/L) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
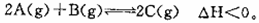 达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是 ( )
达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是 ( )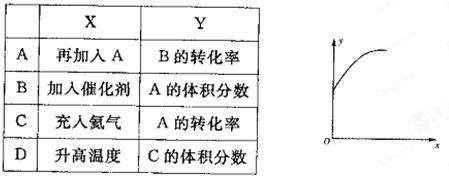
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
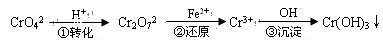
 Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O Cr3+(aq)+3OH—(aq)
Cr3+(aq)+3OH—(aq)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com