
| A. | 用苯从溴水中萃取溴、氯化钠潮解 | B. | 海水蒸馏制淡水、石油裂化 | ||
| C. | 碘的升华、煤的气化 | D. | 石油分馏得到汽油、SO2漂白草帽 |
分析 化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成.
解答 解:A.用苯从溴水中萃取溴,是溴从水中转移到苯中,没有新物质生成,氯化钠潮解是吸收空气中水蒸气在表面形成溶液,都不属于化学变化,故A错误;
B.海水蒸馏制淡水是利用沸点不同分离混合物属于物理变化,石油裂化是大分子分解生成小分子属于化学变化,故B错误;
C.碘的升华属于物理变化,煤的气化是碳变化为一氧化碳和氢气,过程中有新物质生成属于化学变化,故C错误;
D.石油分馏得到汽油是利用沸点不同分离混合物,SO2漂白草帽是 有色物质结合为无色物质发生化学变化,故D错误;
故选A.
点评 本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:解答题
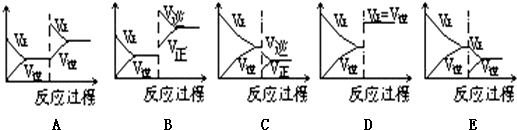
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 物质 | 单晶桂 | 漂白液 | 小苏打 | 铁红 |
| 有效成分 | Si | NaClO | NaHCO3 | Fe2O3 |
| 用途 | 做光导纤维 | 做消毒剂 | 灭火器 | 做涂料 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
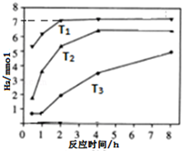 天然气(主要成分甲烷)含有少量含硫化合物[硫化氢、羰基硫(COS)等],可以用氢氧化钠溶液洗涤除去.羰基硫用氢氧化钠溶液处理的过程如下(部分产物已略去):
天然气(主要成分甲烷)含有少量含硫化合物[硫化氢、羰基硫(COS)等],可以用氢氧化钠溶液洗涤除去.羰基硫用氢氧化钠溶液处理的过程如下(部分产物已略去): .反应I除生成两种正盐外,还有水生成,其化学方程式为COS+4NaOH=Na2S+Na2CO3+2H2O.
.反应I除生成两种正盐外,还有水生成,其化学方程式为COS+4NaOH=Na2S+Na2CO3+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| W | 氮 | Y | |
| X | 硫 | Z |
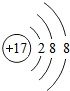 ;写出工业生产X单质粗产品的化学方程式:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO.
;写出工业生产X单质粗产品的化学方程式:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO.查看答案和解析>>
科目:高中化学 来源: 题型:实验题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com