
分析 n(CO2)=$\frac{0.224L}{22.4L/mol}$=0.01mol,n(H2O)=$\frac{0.18g}{18g/mol}$=0.01mol,该物质的蒸气对氢气的相对密度为30,则该有机物的相对分子质量为30×2=60,
6g有机物物质的量$\frac{0.3g}{60g/mol}$=0.005mol,结合原子守恒及质量守恒推断有机物.
解答 解:n(CO2)=$\frac{0.224L}{22.4L/mol}$=0.01mol,n(H2O)=$\frac{0.18g}{18g/mol}$=0.01mol,该物质的蒸气对氢气的相对密度为30,则该有机物的相对分子质量为30×2=60,
6g有机物物质的量$\frac{0.3g}{60g/mol}$=0.005mol,
由原子守恒可知,有机物中C原子个数为$\frac{0.01mol}{0.005mol}$=2,H原子个数为$\frac{0.01mol×2}{0.005mol}$=4,O原子个数为$\frac{\frac{0.3g-0.01mol×12g/mol-0.01mol×2×1g/mol}{16g/mol}}{0.005mol}$=2,
(1)由上述计算可知,1个分子中含2个C、4个H、2个O,则分子式为C2H4O2,
答:有机物的分子式为C2H4O2;
(2)分子式C2H4O2符合羧酸及饱和酯的通式,可能为CH3COOH(乙酸)或HCOOCH3(甲酸甲酯),
答:该有机物可能的结构简式及命名为CH3COOH(乙酸)或HCOOCH3(甲酸甲酯).
点评 本题考查有机物的推断及分子式计算确定,为高频考点,把握守恒法推断分子式及有机物的结构为解答的关键,侧重分析与推断能力、计算能力的考查,题目难度不大.


 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积(mL) | 标准NaOH溶液读数记录(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 4.00 | 24.00 |
| 第三次 | 20.00 | 2.00 | 24.10 |
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 2.0×10-10 | 5.4×10-13 | 8.3×10-17 | 2.0×10-48 | 2.0×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第三周期元素的离子半径从左到右逐渐减小 | |
| B. | ⅥA族元素的原子,其半径越大,越容易得到电子 | |
| C. | ⅥA族元素的氢化物中,稳定性最好的其还原性最强 | |
| D. | IA族与 VIIA族元素间可形成共价化合物或离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
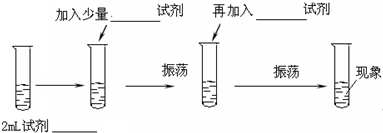
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
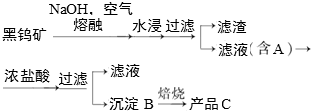
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解合金时收集到NO气体体积为2.24L(在标准状况) | |
| B. | 加入合金的质量不可能为9.6g | |
| C. | 沉淀完全时消耗NaOH溶液的体积为150mL | |
| D. | 参加反应的硝酸的物质的量为0.4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2与酸、碱均不反应 | |
| B. | NO2溶于水时发生氧化还原反应 | |
| C. | SO2具有氧化性,可用于漂白纸浆 | |
| D. | Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 甲中负极反应式为Zn-2e-═Zn2+ | |
| B. | 乙中阳极反应式为Ag-e-═Ag+ | |
| C. | 丙中H+向碳棒方向移动 | |
| D. | 丁中电解开始时阳极产生黄绿色气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com