
·ÖĪö £Ø1£©16g ŅŗĢ¬¼×“¼ĶźČ«Č¼ÉÕ£¬µ±»Öø“µ½ŌדĢ¬Ź±£¬·Å³ö369.2kJµÄČČĮ棬Ōņ1mol ŅŗĢ¬¼×“¼ĶźČ«Č¼ÉÕ£¬µ±»Öø“µ½ŌדĢ¬Ź±£¬·Å³ö725.8kJµÄČČĮ棬¾Ż“ĖŹéŠ“£»
£Ø2£©¼×“¼·¢ÉśŃõ»Æ·“Ó¦£¬ŌŚ¼īŠŌĢõ¼žĻĀÉś³ÉĢ¼ĖįøłĄė×ÓÓėĖ®£»
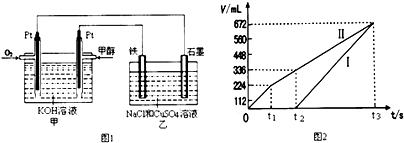
£Ø3£©µē³ŲĶØČė¼×“¼µÄĪŖøŗ¼«£¬ŅŅÖŠĢśµē¼«ĪŖŅõ¼«”¢ŹÆÄ«µē¼«ĪŖŃō¼«£¬æŖŹ¼Cl-ŌŚŃō¼«·ÅµēÉś³ÉĀČĘų£¬Ņõ¼«Cu2+·ÅµēÉś³ÉCu£¬¹ŹĶ¼3ÖŠ¢ń±ķŹ¾Ņõ¼«²śÉśµÄĘųĢ壬¢ņ±ķŹ¾Ńō¼«²śÉśµÄĘųĢ壬Ńō¼«t1Ē°µē¼«·“Ó¦Ź½ĪŖ£ŗ2Cl--4e-=Cl2”ü£¬t1”«t3µē¼«·“Ó¦Ź½ĪŖ£ŗ4OH--4e-=O2”ü+2H2O£¬Ņõ¼«t2Ē°µē¼«·“Ó¦Ź½ĪŖ2Cu2++4e-=2Cu£¬t2µćŗóµē¼«·“Ó¦Ź½ĪŖ4H++4e-=2H2”ü£»
£Ø4£©øł¾Żt1”«t2 Ńō¼«ÉĻÉś³ÉĀČĘųŗĶŃõĘų£¬½įŗĻµĆŹ§µē×ÓŹŲŗć¼ĘĖćCuSO4µÄĪļÖŹµÄĮæÅØ¶Č£®
½ā“š ½ā£ŗ£Ø1£©16g ŅŗĢ¬¼×“¼ĶźČ«Č¼ÉÕ£¬µ±»Öø“µ½ŌדĢ¬Ź±£¬·Å³ö369.2kJµÄČČĮ棬Ōņ1mol ŅŗĢ¬¼×“¼ĶźČ«Č¼ÉÕ£¬µ±»Öø“µ½ŌדĢ¬Ź±£¬·Å³ö725.8kJµÄČČĮ棬¼“ČČ»Æѧ·½³ĢŹ½ĪŖ£ŗCH3OH£Øl£©+$\frac{3}{2}$O2=CO2£Øg£©+2H2O£Øl£©”÷H=-725.8kJ/mol£¬
¹Ź“š°øĪŖ£ŗCH3OH£Øl£©+$\frac{3}{2}$O2=CO2£Øg£©+2H2O£Øl£©”÷H=-725.8kJ/mol£»
£Ø2£©ŌŚČ¼ĮĻµē³ŲµÄÖŠ£¬øŗ¼«ÉĻŹĒČ¼ĮĻ·¢ÉśŹ§µē×ÓµÄŃõ»Æ·“Ó¦£¬ŌŚ¼īŠŌ»·¾³ĻĀ£¬¼×“¼Ź§µē×ӵĹż³ĢĪŖ£ŗCH3OH-6e-+8OH-=CO32-+6H2O£¬
¹Ź“š°øĪŖ£ŗCH3OH-6e-+8OH-=CO32-+6H2O£»
£Ø3£©µē³ŲĶØČė¼×“¼µÄĪŖøŗ¼«£¬ŅŅÖŠĢśµē¼«ĪŖŅõ¼«”¢ŹÆÄ«µē¼«ĪŖŃō¼«£¬æŖŹ¼Cl-ŌŚŃō¼«·ÅµēÉś³ÉĀČĘų£¬Ņõ¼«Cu2+·ÅµēÉś³ÉCu£¬¹ŹĶ¼3ÖŠ¢ń±ķŹ¾Ņõ¼«²śÉśµÄĘųĢ壬¢ņ±ķŹ¾Ńō¼«²śÉśµÄĘųĢ壬Ńō¼«t1Ē°µē¼«·“Ó¦Ź½ĪŖ£ŗ2Cl--4e-=Cl2”ü£¬t1”«t3µē¼«·“Ó¦Ź½ĪŖ£ŗ4OH--4e-=O2”ü+2H2O£¬Ņõ¼«t2Ē°µē¼«·“Ó¦Ź½ĪŖ2Cu2++4e-=2Cu£¬t2µćŗóµē¼«·“Ó¦Ź½ĪŖ4H++4e-=2H2”ü£¬ĖłŅŌĢśµē¼«ÉĻ·“Ó¦µÄĻÖĻóĪŖ£ŗĻČÓŠŗģÉ«µÄĪļÖŹĪö³ö£¬ŗóÓŠĘųÅŻ²śÉś£»ŹÆÄ«µē¼«ÉĻ²śÉśµÄĘųĢåŹĒCl2”¢O2£¬¹Ź“š°øĪŖ£ŗÓŠĘųÅŻ²śÉś£»Cl2”¢O2£»
£Ø4£©ŹÆÄ«ĪŖŃō¼«”¢Ģśµē¼«ĪŖŅõ¼«£¬æŖŹ¼Cl-ŌŚŃō¼«·ÅµēÉś³ÉĀČĘų£¬Ņõ¼«Cu2+·ÅµēÉś³ÉCu£¬¹ŹĶ¼3ÖŠ¢ń±ķŹ¾Ņõ¼«²śÉśµÄĘųĢ壬¢ņ±ķŹ¾Ńō¼«²śÉśµÄĘųĢ壬t1Ē°µē¼«·“Ó¦Ź½ĪŖ£ŗŃō¼«2Cl--4e-=Cl2”ü£¬t2µćŗóµē¼«·“Ó¦Ź½ĪŖ£ŗŃō¼«4OH--4e-=O2”ü+2H2O£¬
ÓÉĶ¼æÉÖŖ£¬²śÉśĀČĘųĪŖ224mL£¬ŌņÓÉ2Cl--2e-=Cl2”üæÉÖŖ£¬n£ØNaCl£©=$\frac{0.224L}{22.4L/mol}$”Į2=0.02mol£¬ÓÉt2Ź±Éś³ÉŃõĘųĪŖ112mL£¬n£ØO2£©=$\frac{0.112L}{22.4L/mol}$=0.005mol£¬Ōņ¹²×ŖŅʵē×ÓĪŖ0.02mol+0.005mol”Į4=0.04mol£¬
øł¾Żµē×ÓŹŲŗć¼°Cu2++2e-=CuæÉÖŖ£¬n£ØCuSO4£©=$\frac{0.04mol}{2}$=0.02mol£¬ĖłŅŌc£ØCuSO4£©=$\frac{0.02mol}{0.2L}$=0.1mol/L£¬
¹Ź“š°øĪŖ£ŗ0.1£®
µćĘĄ ±¾Ģāæ¼²éµē½āŌĄķ£¬Ć÷Č··¢ÉśµÄµē¼«·“Ó¦¼°Ķ¼Ķ¼ĻóµÄ¶ŌÓ¦¹ŲĻµŹĒ½ā“š±¾ĢāµÄ¹Ų¼ü£¬¼ĘĖćׄהĮ½¼«µē×Ó×ŖŅĘĻąµČ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃ鱹ŗÅ | HAĪļÖŹµÄĮæÅØ¶Č£Ømol/L£© | NaOHĪļÖŹµÄĮæÅØ¶Č£Ømol/L£© | »ģŗĻČÜŅŗµÄpH |
| ¼× | 0.2 | 0.2 | pH=a |
| ŅŅ | c1 | 0.2 | pH=7 |
| ±ū | 0.1 | 0.1 | pH£¾7 |
| ¶” | 0.1 | 0.1 | pH=9 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2O2ÓĆ×÷ŗōĪüĆę¾ßµÄ¹©Ńõ¼Į | B£® | ¹¤ŅµÉĻµē½āČŪȌדĢ¬Al2O3ÖʱøAl | ||
| C£® | ¹¤ŅµÉĻĄūÓĆŗĻ³É°±ŹµĻÖČĖ¹¤¹ĢµŖ | D£® | ŹµŃéŹŅÓĆNH4Cl ŗĶCa£ØOH£©2ÖʱøNH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | DŗĶT»„ĪŖĶ¬Ī»ĖŲ | B£® | C2H6ŗĶCH3CH2CH2CH3»„ĪŖĶ¬ĻµĪļ | ||
| C£® | C£® Óė Óė »„ĪŖĶ¬·ÖŅģ¹¹Ģå »„ĪŖĶ¬·ÖŅģ¹¹Ģå | D£® | O2ŗĶO3»„ĪŖĶ¬ĖŲŅģŠĪĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | øĆ×°ÖĆĪŖŌµē³Ų£¬ĒŅĶĪŖÕż¼« | |
| B£® | µē³Ų¹¤×÷Ź±£¬H+ĻņCuµē¼«ŅĘ¶Æ | |
| C£® | GaNµē¼«±ķĆęµÄµē¼«·“Ó¦Ź½ĪŖ£ŗ2H2O-4e-ØTO2+4H+ | |
| D£® | ·“Ó¦CO2+2H2OØTCH4+2O2ÖŠĆæĻūŗÄ1mol CO2×ŖŅĘ4mol e- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “óĮæÅŷŵŖŃõ»ÆĪļæÉŅŌŠĪ³ÉĖįÓź”¢²śÉś¹ā»ÆѧŃĢĪķ£¬ĶžŠ²ČĖĄąÉś»ī»·¾³ | |
| B£® | Ź³ÓƵŲ¹µÓĶ¶ŌČĖĢåĪ£ŗ¦“󣬵«µŲ¹µÓĶæÉÓĆĄ“ÖĘ·ŹŌķ | |
| C£® | Ć÷·ÆĖ®½āæÉÉś³ÉAl£ØOH£©3½ŗĢ壬³£ÓĆÓŚĖ®µÄɱ¾śĻū¶¾ | |
| D£® | ČĖĆĒæÉĄūÓĆŌŖĖŲÖÜĘŚĀÉŌŚ¹ż¶ÉŌŖĖŲÖŠŃ°ÕŅŠŌÄÜÓÅĮ¼µÄ“߻ƼĮ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com