
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
分析 含钴废料中加入盐酸、Na2SO3,可得CoCl2、AlCl3、FeCl2,加入NaClO3,发生氧化还原反应可得到FeCl3,然后加入Na2CO3调pH至5.2,可得到Fe(OH)3、Al(OH)3沉淀,然后过滤,向滤液中加入萃取剂,将锰离子萃取,萃取后的溶液中主要含有CoCl2,为得到CoCl2•6H2O晶体,将溶液蒸发浓缩、冷却结晶,应控制温度在86℃以下,加热时要防止温度过高而失去结晶水,可减压烘干.
(1)酸性条件下,Co2O3和SO32-发生氧化还原反应生成Co2+、SO42-;
(2)将亚铁离子氧化为铁离子,便于转化为氢氧化铁沉淀除去;搅拌进行充分接触、适当延长浸取时间等都可以提高浸取率;实验室用二氧化锰与浓盐酸在加热条件下制备氯气;
(3)“加Na2CO3调pH至a”,目的是除去铁离子、铝离子,所以需要将铁离子、铝离子转化为沉淀;
(4)CoCl2•6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴;
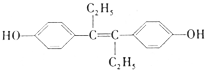
(5)滤液中加入萃取剂的作用是除去锰离子,由表中数据可知,调节溶液PH在3.0~3.5之间,可使Mn2+完全沉淀,并防止Co2+转化为Co(OH)2沉淀;
(6)根据CoCl2•6H2O的组成分析,可能是含有杂质,也可能是失去部分水.
解答 解:含钴废料中加入盐酸、Na2SO3,可得CoCl2、AlCl3、FeCl2,加入NaClO3,发生氧化还原反应可得到FeCl3,然后加入Na2CO3调pH至5.2,可得到Fe(OH)3、Al(OH)3沉淀,过滤后所得滤液主要含有CoCl2,为得到CoCl2•6H2O晶体,应控制温度在86℃以下,加热时要防止温度过高而失去结晶水,可减压烘干.
(1)酸性条件下,Co2O3和SO32-发生氧化还原反应生成Co2+、SO42-,反应离子方程式为:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O,
故答案为:Co2O3+SO32-+4H+=2Co2++SO42-+2H2O;
(2)酸性条件下,将Fe2+氧化为Fe3+,便于调节pH转化氢氧化铁沉淀而除去,
加快搅拌速率、适当延长浸取时间、分数次浸取等都可以提高浸取率,
实验室用二氧化锰与浓盐酸在加热条件下制备氯气,反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案为:将Fe2+氧化为Fe3+;加快搅拌速率、适当延长浸取时间、分数次浸取等;MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(3)“加Na2CO3调pH至a”,目的是除去铁离子、铝离子,将铁离子、铝离子转化为Fe(OH)3、Al(OH)3沉淀,过滤除去,
故答案为:Fe(OH)3、Al(OH)3;
(4)CoCl2•6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴,减压烘干目的是:降低烘干温度,防止产品分解
故答案为:降低烘干温度,防止产品分解;
(5)根据流程图可知,此时溶液中存在Mn2+、Co2+金属离子,由萃取剂对金属离子的萃取率与pH的关系可知,调节溶液PH在3.0~3.5之间,可使Mn2+完全沉淀,并防止Co2+转化为Co(OH)2沉淀,
故答案为:除去溶液中的Mn2+;B;
(6)造成产品中CoCl2•6H2O的质量分数大于100%的原因可能是:粗产品含有可溶性氯化物或晶体失去了部分结晶水,导致相同质量的固体中氯离子含量变大,
故答案为:粗产品含有可溶性氯化物或晶体失去了部分结晶水.
点评 本题属于化学工艺流程题目,涉及物质分离和提纯、对操作与药品的分析评价、元素化合物知识、含量测定误差分析、信息获取与迁移运用等,关键是理解工艺流程,题目难度中等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 稀盐酸 | MnO2 | 石蕊溶液 | 石蕊溶液先变红后褪色 | |
| B | 浓硫酸 | 蔗糖 | 品红 | 浓硫酸有脱水性、氧化性 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | 生成BaSO3白色沉淀 | |
| D | 醋酸 | Na2CO3 | 苯酚钠溶液 | 酸性:醋酸>碳酸>苯酚 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以用有机溶剂萃取 | |
| B. | 可与NaOH或NaHCO3溶液发生反应 | |
| C. | 1mol该有机物可以与5molBr2发生反应 | |
| D. | 该有机物分子中,可能有8个碳原子共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 乙炔是一种重要的有机物化工原料,现以它为原料,设计如下转化关系图(部分产物、反应条件已略去),其中A是由等物质的量的乙炔、一氧化碳和水反应而得.
乙炔是一种重要的有机物化工原料,现以它为原料,设计如下转化关系图(部分产物、反应条件已略去),其中A是由等物质的量的乙炔、一氧化碳和水反应而得. 不稳定,会自动转化R-CH2CHO.请回答:
不稳定,会自动转化R-CH2CHO.请回答: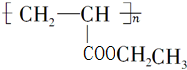 .
.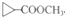 是D的一种同分异构体
是D的一种同分异构体查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高温煅烧石灰石的反应中,反应物总能量高于生成物总能量 | |
| B. | 中和反应中,反应物总能量高于生成物总能量 | |
| C. | 铝粉和盐酸反应时,溶液温度通常会上升 | |
| D. | 氢氧化钡晶体和氯化铵晶体的反应是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
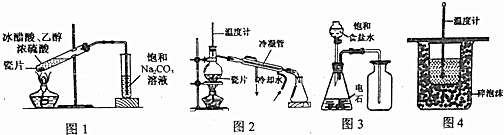
| A. | 用图1装置制取少量乙酸乙酯 | B. | 用图2装置分离苯和溴苯 | ||
| C. | 用图3装置制取并收集乙炔气体 | D. | 用图4装置测定中和热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH、KOH、RbOH的碱性逐渐增强 | B. | HCl、H2S、PH3的稳定性逐渐减弱 | ||
| C. | Na、K、Rb的原子半径依次增大 | D. | HF、HCl、HBr、HI的稳定性逐渐增强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com