
分析 1molO2只有0.3mol转化为0.2molO3,反应后气体的总物质的量为0.7mol+0.2mol=0.9mol,结合M=$\frac{m}{n}$、d=$\frac{{M}_{混}}{{M}_{氢气}}$计算.
解答 解:由反应及信息可知,1molO2只有0.3mol转化为0.2molO3,反应后气体的总物质的量为0.7mol+0.2mol=0.9mol,
(1)放电后混合气体的平均摩尔质量为$\frac{32g}{0.9mol}$=35.56g/mol,
答:放电后混合气体的平均摩尔质量为35.56g/mol;
(2)放电后混合气体对H2的相对密度为$\frac{35.56}{2}$=17.78,
答:放电后混合气体对H2的相对密度为17.78.
点评 本题考查物质的量的计算,为高频考点,把握平均摩尔质量、相对密度的计算方法为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | c(H+)等于1×10-7 mol•L-1的溶液一定是中性溶液 | |
| B. | 0.2 mol•L-1 CH3COOH溶液中的c(H+)是0.1 mol•L-1 CH3COOH溶液中的c(H+)的2倍 | |
| C. | 室温时,pH=2的CH3COOH和0.01 mol•L-1 NaOH溶液等体积混合,混合后pH=7 | |
| D. | 等物质的量浓度的Na2S和NaHS混合溶液中:2c(Na+)=3[c(S2-)+c(HS-)+c(H2S)] |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
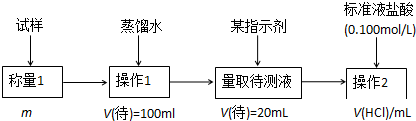
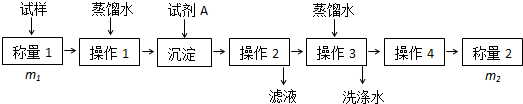
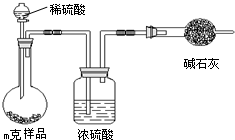
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通H2的一极是正极,通O2的一极是负极 | |
| B. | 通O2的一极是正极,通H2的一极是负极 | |
| C. | 工作一段时间后电解质溶液pH增大 | |
| D. | 工作时负极区附近pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
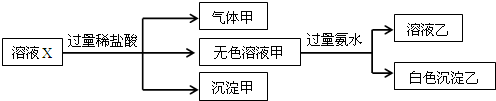
| A. | 气体甲一定是纯净物 | |
| B. | 沉淀甲是硅酸和硅酸铝的混合物 | |
| C. | 所有阴离子都可能存在于溶液X中 | |
| D. | 沉淀乙可能是Mg(OH)2和Al(OH)3的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X气体的相对分子质量比Y气体的相对分子质量大 | |
| B. | X可能是C2H4,Y可能是CH4 | |
| C. | X气体的密度小于Y气体的密度 | |
| D. | 充气后A气球质量比B气球质量大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将金粉和铁粉混合 | B. | 将牛奶加入水中混合 | ||
| C. | 蒸发食盐水制取食盐晶体 | D. | 用漏斗、滤纸过滤除去水中的泥沙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com