
(15分)对下图中两极加以必要的连接并填空:

(1)在图A中,使铜片上产生氢气。
①若加以导线连接,则连接后的装置叫 (填“原电池”或“电解池”)。锌片发生 (填“氧化”或“还原”);铜片上的电极反应式: 。
②若外加电源,则连接后的装置叫 (填“原电池”或“电解池”),其中铜片作为该装置的 极,连接电源的 极;锌片上发生的电极反应式为 。
(2)在图B中,使a极析出铜。
①若a、b电极均为石墨电极并加以必要的连接,则连接后的装置应为 (填“原电池”或“电解池”);该装置工作时,溶液中阴离子向 极作定向移动(填“a”或“b”); 经过一段时间后,停止反应并搅匀溶液,溶液的酸性 (填“增强”、“降低”或“不变”)。
②若a、b电极加以导线连接,且a极为铜电极,则b极可以为 电极(填序号)。A.铂 B.铁 C.石墨 D.银 E.锌
该装置工作时,溶液中阴离子向 极作定向移动(填“a”或“b”)。
(1) ①原电池(1分);氧化(1分);2H+ + 2e-= H2↑(2分)
②电解池(1分);阴极(1分);负极(1分);Zn - 2e- = Zn2+ (2分)
(2) ①电解池(1分); b(1分);增强(1分)
②B、E (2分); b(1分)。
【解析】(1)①由于铜不能和稀硫酸反应生成氢气,所以要使铜片上产生氢气,则必须通过原电池或电解池实现;如果是原电池,由于锌比铜活泼,锌是负极失去电子。铜是正极,溶液中的氢离子得到电子,电极反应式是2H+ + 2e-= H2↑。
②外加电源,则连接后的装置叫电解池。此时铜应该和电源的负极相连,作阴极氢离子放电。锌和电源的正极相连,作阳极,失去电子,电极反应式是Zn - 2e- = Zn2+。
(2)①由于a、b电极均为石墨电极,所以是利用电解池实现的。要使a极析出铜,则a电极必须是阴极,和电源的负极相连。则b电极就是阳极,电解池中阴离子向阳极移动。所以溶液中阴离子向b极作定向移动;阳极是OH-放电生成氧气,阴极是铜离子放电析出铜,所以还有硝酸生成,溶液的酸性是增强的。
②若a、b电极加以导线连接,则是通过原电池实现的。要使a极析出铜,则a电极必须是正极,所以b电极的金属性要强于a电极的,因此正确的答案选BE;原电池中溶液中阴离子向负极移动,即向b电极移动。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:阅读理解
(本题共15分)你注意到汽车加油站内的标牌了吗?某些省市加油站提供的汽油标号由90号、93号换成了E90、E93,后者是在汽油中加入了10%的燃料乙醇而制得的乙醇汽油。
燃料乙醇的生产过程可由下图表示:
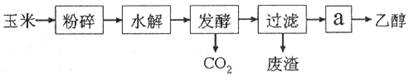
(1)粉碎玉米的目的是: 。
(2)生产过程中为了检验淀粉水解是否完全,可使用试剂是 。
(3)步骤a的操作是( )。
A、蒸发 B、萃取 C、蒸馏 D、分液
(4)发酵产生的CO2纯度可达到99%,能回收利用,请举出它的两项用途: 。
(5)以玉米等淀粉原料生产乙醇的化学反应可用下式表示:
根据上述反应式,可以算出100kg淀粉理论上可生产无水乙醇 kg。(相对原子质量:C-12 H-1 O-16)
到目前为止,我国已有上百个地市使用乙醇汽油。
(1)为了便于区分燃料乙醇和食用乙醇,常在燃料乙醇中添加少量煤油,这里利用了煤油的物理性质是: 。
(2)含10%乙醇的汽油在储存和运输过程中应特别注意防水,如果混入了水,汽油中会出现的现象是 。
右图是燃料乙醇的生产和消费过程示意图。虽然燃料乙醇的使用缓解了汽车能源的紧张状况,但仍存在一些问题。由此可知,燃料乙醇( )
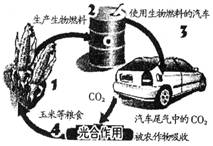
A、是最理想的绿色能源
B、提供的能量来自于太阳能
C、生产和消费过程对空气没有任何影响
D、生产过程中将消耗大量粮食,以避免粮食过剩
除了燃料乙醇,二甲醚(CH3OCH3)和甲醇(CH3OH)也可作为汽车燃料,其中与乙醇互为同分异构体的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(15分)
我国有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某
些转化步骤及生成物未列出):
请填写下列空白:
(1)已知0.5 mol甲烷和0.5 mol水蒸气在t ℃,p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量。该反应的热化学方程式是: ______。
(2)上述流程中,工业上分离H2 、CO2合理的方法是___________。
A.混合气先通入氢氧化钠溶液,再在溶液中加盐酸
B.混合气加压冷却,使CO2液化
C.混合气用氨水洗涤
D.混合气先通入到石灰浆,然后高温煅烧固体,
(3)为了保证氨气顺利合成,在空气进入合成塔之前必须对空气进行___________,目的是________________________________________;在合成氨的实际生产过程中,常采取将生成的氨从混合气体中分离出来,分离出氨的方法: 。
(4)合理地利用资源不仅可以提高经济效益,而且也是对社会、对全人类负责的表现,请用线段和箭头画出图中的两处合理利用资源情况。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年黑龙江省高三上学期开学考试化学试卷(解析版) 题型:填空题
(15分)1、下列有关元素锗及其化合物的叙述中正确的是 ___________
A.锗的第一电离能高于碳而电负性低于碳
B.四氯化锗与四氯化碳分子都是四面体构型
C.二氧化锗与二氧化碳都是非极性的气体化合物
D.锗和碳都存在具有原子晶体结构的单质
2、铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域。回答下列问题:
(1)铜原子基态电子排布式为 ;
(2)用晶体的x射线衍射法可以测得阿伏加德罗常数。对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为361pm。又知铜的密度为9.00g·cm-3,则阿伏加德罗常数为 (列式计算);
(3)氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如下图),a位置上Cl原子的杂化轨道类型为 。已知其中一种化合物的化学式为KCuCl3,另一种的化学式为 ;
(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是 ,反应的化学方应程式为 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年辽宁省高三下学期模拟考试(理综)化学部分 题型:实验题海水资源
(15分)
沿海地区有着丰富的海水资源,海水占地球总储水量的97.4﹪,海水是人类宝贵的自然资源,若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海水资源,从海水中可以提取多种化工原料,下图是某工厂对海水资源综合利用的示意图:
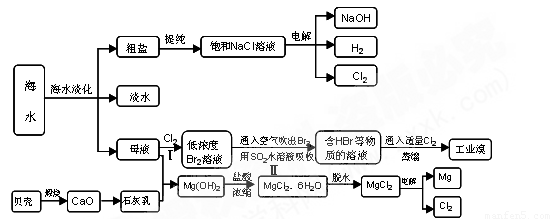
⑴请列举海水淡化的两种方法 、 。
⑵使用离子交换树脂与水中的离子进行交换也是常用的水处理技术。聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式 .
⑶步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br -,其目的是: .
步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式
⑷在制取无水氯化镁时需要在干躁的HCl气流中加热MgCl2.6H2O的原因
.
⑸电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用做镁蒸气的冷却剂的是
A.H2 B.CO2 C.空气 D.O2 E.水蒸气
⑹苦卤(海水蒸发结晶分离出食盐后的母液)中含有较多的NaCl、MgCl2、KCl、MgSO4等物质.用沉淀法测定苦卤中MgCl2的含量(g/L),测定过程中应获取的数据有
.
查看答案和解析>>
科目:高中化学 来源:2010-2011学年吉林省长春市高三第二次模拟考试(理综)化学部分 题型:填空题
(15分)
我国有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某
些转化步骤及生成物未列出):

请填写下列空白:
(1)已知0.5 mol甲烷和0.5 mol水蒸气在t ℃,p k Pa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量。该反应的热化学方程式是: ______。
(2)上述流程中,工业上分离H2 、CO2合理的方法是___________。
A.混合气先通入氢氧化钠溶液,再在溶液中加盐酸
B.混合气加压冷却,使CO2液化
C.混合气用氨水洗涤
D.混合气先通入到石灰浆,然后高温煅烧固体,
(3)为了保证氨气顺利合成,在空气进入合成塔之前必须对空气进行___________,目的是________________________________________;在合成氨的实际生产过程中,常采取将生成的氨从混合气体中分离出来,分离出氨的方法: 。
(4)合理地利用资源不仅可以提高经济效益,而且也是对社会、对全人类负责的表现,请用线段和箭头画出图中的两处合理利用资源情况。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com