
有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数),下列说法正确的是()
A. 若X(OH)n为强碱,则Y(OH)n也一定为强碱
B. 若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C. 若X形成的单质是X 2,则Y元素形成的单质一定是Y2
2,则Y元素形成的单质一定是Y2
D. 若Y的最高正价为+m,则X的最高正价一定为+m
考点: 原子结构与元素的性质.
专题: 元素周期律与元素周期表专题.
分析: X、Y原子的最外层电子数相同,说明位于同一主族,X的原子半径小于Y,则原子序数Y大于X,根据同主族元素性质的递变规律判断.
解答: 解:X、Y原子的最外层电子数相同,说明位于同一主族,X的原子半径小于Y,则原子序数Y大于X,则:
A.如X、Y为金属元素,同主族元素从上到下元 素的金属性逐渐增强,对应的最高价氧化物的水化物的碱性逐渐增强,故A正确;
素的金属性逐渐增强,对应的最高价氧化物的水化物的碱性逐渐增强,故A正确;
B.若HnXOm为硝酸,则X的氢化物为氨气,为碱性气体,溶于水呈碱性,故B错误;
C.若X形成的单质是N2,则Y元素形成的单质可以是红磷或者白磷,白磷的分子式为P4,故C错误;
D.若Y的最高正价为+m,X不一定有正价,如Cl的最高正价为+7价,而F的最高价为0价,故D错误.
故选A.
点评: 本题考查原子结构与元素的性质,题目难度不大,本题注意同主族元素性质的递变规律,特别注意化合价等问题.


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
下列两个热化学方程式:2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJ/mol;C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=2 220kJ/mol.现有H2和C3H8的混合气体共5mol,完全燃烧时放热3 847kJ,则在混合气体中H2和C3H8的体积比是()
A. 2:1 B. 3:1 C. 4:1 D. 5:1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. H、D、T属于同位素,H2、D2、T2属于同素异形体
B. 氯水、氨水、王水是混合物,水银、水玻璃是纯净物
C. HCl、NH3、BaSO4是电解质,CO2、Cl2、CH3CH2OH是非电解质
D. 水能、风能、生物质能是可再生能源,煤、石油、天然气是不可再生能源
查看答案和解析>>
科目:高中化学 来源: 题型:
某强酸性溶液X中可能含有Fe2+、A13+、NH4+、CO32﹣、SO32﹣、SO42﹣、C1﹣中的若干种,现取X溶液进行连续实验,实验过程及产物如图.下列说法正确的是()
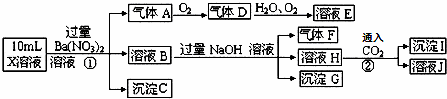
A. 气体A是NO2
B. X中肯定存在Fe2+、A13+、NH4+、SO42﹣
C. 溶液E和气体F不能发生化学反应
D. X中不能确定的离子是 A13+和C1﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价有+l、+2.已知Cu2O与稀硫酸反应,溶液呈蓝色.现向Cu、Cu2O和CuO组成的混合物中,加入1L 0.6mol/L HNO3溶液恰好使混合物溶解,同时收集到2240mL NO气体(标准状况).请回答下列问题:
(1)写出Cu2O跟稀硝酸反应的离子方程式
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为 .
(3)若混合物中含0.1mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物质的量为 .
(4)若混合物中Cu的物质的量为n mol,则n的取值范围为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
沼气是一种能源,它的主要成分是CH4,0.5molCH4完全燃烧生成CO2和液态水时放出445kJ的热最,则下列热化学方程式中正确的是()
A. 2CH4(g)+4O2(g)=2CO2(g)+4H2O(g)△H=+890kJ•mol﹣1
B. CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890kJ•mol﹣1
C. CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣890kJ•mol﹣1
D. 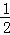 CH4(g)+O2(g)=CO2(g)+H2O(l)△H=﹣890kJ•mol﹣1
CH4(g)+O2(g)=CO2(g)+H2O(l)△H=﹣890kJ•mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据你所掌握的电镀原理,你认为在硬币制作时,钢芯应做()
A. 阴极 B. 阳极 C. 正极 D. 负极
查看答案和解析>>
科目:高中化学 来源: 题型:
已知前四周期五种元素X、Y、Z、W、T,它们的原子序数依次增大.X是空气中含量最多的元素;Y、W位于同周期,W单质在常温下是黄绿色气体,Y单质在其中燃烧发出黄色火焰;Z的氧化物常用作制备通讯光纤;T是常见金属,在氧气中燃烧可以得到具有磁性的黑色物质.回答下列问题:
(1)Z位于元素周期表中第三周期第ⅣA族;W基态原子核外电子排布式为 .
(2)Y和W的简单离子比较,半径较大的是 (填离子符号);键的极性比较:X﹣H Z﹣H(填“大于”或“小于”);Z单质和其氧化物比较,熔点较高的是 (填化学式).
(3)向T单质与稀硫酸反应后的溶液中滴加足量的NaOH溶液,能观察到的现象是 ;X与Y形成的原子个数比为1:3的简单化合物可与水反应生成两种碱,写出该物质与醋酸溶液反应的化学方程式 .
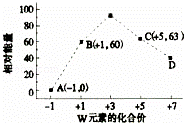
(4)一定条件下,在水溶液中1molW﹣、WO (z=1,2,3,4等)的能量(kJ)相对大小如图所示.
(z=1,2,3,4等)的能量(kJ)相对大小如图所示.
①D点对应的微粒是ClO4﹣(填离子符号).
②写出B→A+C反应的热化学方程式: (用离子符号表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
充分燃烧一定量丁烷气体放出的热量为Q,完全吸收它生成的CO2生成正盐,需要5mol•L﹣1 的KOH溶液100mL,则丁烷的燃烧热为()(单位:kJ/mol)
A. 16Q B. 8Q C. 4Q D. 2Q
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com