
| A£® | ĶµÄ½šŹō»ī¶ÆŠŌ±ČĢś²ī£¬æÉŌŚŗ£ĀÖĶāæĒÉĻ×°ČōøÉĶæéŅŌ¼õ»ŗĘäøÆŹ“ | |
| B£® | ļ§ŃĪŹÜČČŅ×·Ö½ā£¬ŹµŃéŹŅ³£¼ÓČČĻõĖįļ§ÓėĒāŃõ»ÆøʵĻģŗĻĪļÖĘČ”°±Ęų | |
| C£® | ĀČ»ÆĢśÓŠŃõ»ÆŠŌ£¬¹¤ŅµÉĻÓĆFeCl3ČÜŅŗŹ“æĢĶ²ÖĘŌģµēĀ·°å | |
| D£® | °±Ė®¾ßÓŠČõ¼īŠŌ£¬æÉÓė±„ŗĶĀČ»ÆĢśČÜŅŗ·“Ó¦ÖʵĆĒāŃõ»ÆĢś½ŗĢå |
·ÖĪö A”¢øł¾ŻĪžÉüŃō¼«µÄŅõ¼«±£»¤·ØĄ“±£»¤½šŹō£»
B”¢ĻõĖįļ§ŹÜČČŅ×·Ö½ā±¬ÕØ£»
C”¢FeCl3ÄÜŗĶĶ·“Ó¦£»
D”¢FeCl3ŗĶ°±Ė®Éś³ÉµÄŹĒĒāŃõ»ÆĢś³Įµķ£®
½ā“š ½ā£ŗA”¢½«ĶĮ¬ŌŚĀÖ“¬ÉĻ£¬ŌņĶ×öÕż¼«£¬ĀÖ“¬×öøŗ¼«£¬»į¼ÓæģĀÖ“¬µÄøÆŹ“£»ŅņŅŖ¼õ»ŗ“¬ĢåµÄøÆŹ“Ó¦Į¬½Ó±ČĢśøü»īĘĆµÄ½šŹō£¬ČēŠæ£¬Õā¾ĶŹĒĪžÉüŃō¼«µÄŅõ¼«±£»¤·Ø£¬¹ŹA“ķĪó£»
B”¢ļ§ŃĪÓė¼ī·“Ӧɜ³É°±ĘųŠčŅŖ¼ÓČČ£¬¶ųĻõĖįļ§ŹÜČČŅ×·Ö½ā±¬ÕØ£¬ĖłŅŌ²»ÄÜÓĆĻõĖįļ§Óė¼ī¼ÓČČ·“Ó¦Öʱø°±Ęų£¬ŹµŃéŹŅ³£¼ÓČČĀČ»Æļ§ÓėĒāŃõ»ÆøʵĻģŗĻĪļÖʱø°±Ęų£¬¹ŹB“ķĪó£»
C”¢FeCl3ÄÜŗĶĶ·“Ó¦£ŗ2FeCl3+Cu=2FeCl2+CuCl2£¬¹ŹÄÜøÆŹ“Ó”Ė¢µēĀ·°å£¬¹ŹCÕżČ·£»
D”¢FeCl3ŗĶ°±Ė®Éś³ÉµÄŹĒĒāŃõ»ÆĢś³Įµķ£¬µĆµ½µÄ²»ŹĒ½ŗĢ壬ŅŖĻėµĆµ½½ŗĢ壬Ӧ½«ĀČ»ÆĢśČÜŅŗµĪČė·ŠĖ®ÖŠ£¬¹ŹD“ķĪó£®
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖļ§ŃĪµÄŠŌÖŹ”¢°±ĘųµÄÖʱø”¢øÖĢśµÄøÆŹ“·Ą»¤£¬ĢāÄæÄŃ¶Č²»“ó£¬ŹōÓŚ»ł“”ŠŌÖŖŹ¶µÄ漲飬²ąÖŲÓŚæ¼²éѧɜ¶Ō»ł“”ÖŖŹ¶µÄÓ¦ÓĆÄÜĮ¦£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 Ņ»¶ØĪĀ¶ČĻĀ£¬½«0.4mol SO2ŗĶ0.2mol O2·ÅČė¹Ģ¶ØČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©”÷H=-196.6kJ/mol£¬·“Ó¦ÖŠSO3µÄĪļÖŹµÄĮæÅØ¶ČµÄ±ä»ÆĒéæöČēĶ¼£ŗ
Ņ»¶ØĪĀ¶ČĻĀ£¬½«0.4mol SO2ŗĶ0.2mol O2·ÅČė¹Ģ¶ØČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©”÷H=-196.6kJ/mol£¬·“Ó¦ÖŠSO3µÄĪļÖŹµÄĮæÅØ¶ČµÄ±ä»ÆĒéæöČēĶ¼£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | pH=4.0µÄ·¬ĒŃÖÖŠc£ØH+£©ŹĒpH=6.0µÄÅ£ÄĢÖŠc£ØH+£©µÄ100±¶ | |
| B£® | Ēæµē½āÖŹČÜŅŗµÄµ¼µēŠŌŅ»¶Ø±ČČõµē½āÖŹČÜŅŗµÄµ¼µēŠŌĒæ | |
| C£® | AgClŌŚĶ¬ÅØ¶ČµÄCaCl2ŗĶNaClČÜŅŗÖŠµÄČܽā¶ČĻąĶ¬ | |
| D£® | pH=5.6µÄCH3COOHÓėCH3COONa»ģŗĻČÜŅŗÖŠ£¬c£ØNa+£©£¾c£ØCH3COO-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ²Ł ×÷ | ĻÖ Ļó |
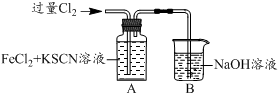 | I£®AÖŠČÜŅŗ±äŗģ II£®ÉŌŗó£¬ČÜŅŗÓÉŗģÉ«±äĪŖ»ĘÉ« |
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ż | B£® | ¢Ū¢Ž | C£® | ¢Ł¢Ś¢Ü | D£® | ¢Ś¢Ü¢Ż¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £Ø»ņ
£Ø»ņ
 £©£®
£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČāĄąø»ŗ¬µ°°×ÖŹ£¬ŹōÓŚ¼īŠŌŹ³Īļ | |
| B£® | Ģ¼ĖįĒāÄĘæÉÓĆÓŚÖĪĮĘĪøĖį¹ż¶ą | |
| C£® | µāŹĒČĖĢå±ŲŠčµÄĪ¢ĮæŌŖĖŲÖ®Ņ» | |
| D£® | Ź³ÓĆø»ŗ¬Ī¬ÉśĖŲCµÄĖ®¹ūÓŠŅęÓŚÉķĢå½”æµ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | KOH ČÜŅŗÓėFeCl3 ČÜŅŗ¼Ó×ćĮæĻ”ĻõĖį | |
| B£® | Ba£ØOH£©2 ČÜŅŗÓėKNO3ČÜŅŗ¼Ó×ćĮæH2SO4 | |
| C£® | CuSO4ČÜŅŗÓėNaOH ČÜŅŗ¼Ó×ćĮæĻ”ŃĪĖį | |
| D£® | BaCl2 ČÜŅŗÓėNa2CO3 ČÜŅŗ¼Ó×ćĮæĻ”“×Ėį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com