
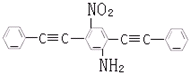
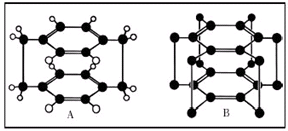
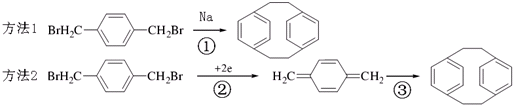
 反应①的类型是:
反应①的类型是:

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
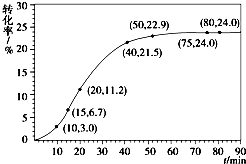 (1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:| 组分 | HCOOCH3 | H2O | HCOOH | CH3OH |
| 物质的量/mol | 1.00 | 1.99 | 0.01 | 0.52 |
查看答案和解析>>
科目:高中化学 来源: 题型:
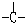 和一个-Cl,它可能的结构有四种,试写出其中的三种结构简式.
和一个-Cl,它可能的结构有四种,试写出其中的三种结构简式.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Si是一种非金属主族元素,其氧化物可用于制作计算机芯片 |
| B、胃穿孔患者胃酸过多时,可服用含Al(OH)3的药片 |
| C、Mg、Fe等金属在一定条件下与水反应都生成H2和对应的氢氧化物 |
| D、铝粉和氧化镁粉末混合,高温能发生铝热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、汽油中混有少量水:用蒸馏的方法除去水 |
| B、除去乙醇溶液中的水,可用蒸馏法 |
| C、分离NaCl溶液中的碘单质,可用蒸馏法 |
| D、从NaCl溶液中得到NaCl固体,可用蒸馏法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com