
| A. | 3,4,4-三甲基己烷 | B. | 3,3-二甲基-2-乙基戊烷 | ||
| C. | 3,3,4-三甲基己烷 | D. | 3,3-二甲基-4-乙基戊烷 |
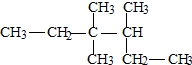
分析 该有机物为烷烃,根据烷烃的命名原则进行解答:
烷烃命名原则:
①长--选最长碳链为主链;
②多--遇等长碳链时,支链最多为主链;
③近--离支链最近一端编号;
④小--支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简--两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面.
解答 解: 该有机物为烷烃,其分子中最长碳链含有6个C,主链为己烷,编号时必须满足取代基的编号之和最小,即:从距离取代基最近的一端开始编号,该有机物应该从左端开始编号,该有机物名称为:3,3,4-三甲基己烷,
该有机物为烷烃,其分子中最长碳链含有6个C,主链为己烷,编号时必须满足取代基的编号之和最小,即:从距离取代基最近的一端开始编号,该有机物应该从左端开始编号,该有机物名称为:3,3,4-三甲基己烷,
故选C.
点评 本题考查了烷烃的命名,题目难度不大,为高考的高频题,侧重对学生基础知识的检验和训练,该题的关键是明确有机物的命名原则,然后结合有机物的结构简式灵活运用即可,有利于培养学生的规范答题能力.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl晶体、BaSO4 | B. | 铝、二氧化硫 | ||
| C. | 液态的醋酸、酒精 | D. | 熔融的KNO3、硫酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | H2 | CO | CH4 |
| 燃烧热(kJ•mol-1) | 285.8 | 283.0 | 890.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4、C2H6O | B. | C2H2、C6H6 | C. | CH2O、C3H6O2 | D. | CH4、C2H4O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 5:7 | D. | 7:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.8mol/(L•s) | B. | 2.0mol/(L•s) | C. | 4.0mol/(L•s) | D. | 6.0mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com