
【题目】下列关于有机化合物的说法正确的是
A. 2-甲基丁烷也称异丁烷
B. 由乙烯生成乙醇属于加成反应
C. C4H9Cl有3种同分异构体
D. 油脂和蛋白质都属于高分子化合物
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列关于金属铬的叙述中不正确的是( )
A. 铬元素在周期表中处于第四周期VIB族
B. 铬原子的外围电子层排布为3d44s2
C. 铬原子中,质子数为24
D. 铬元素位于元素周期表的d区,是过渡元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向1 L含0.01 mol NaAlO2和0.02 mol NaOH的溶液中缓慢通入CO2,随n(CO2)增大,先后发生三个不同的反应,当0.01 mol<n(CO2)![]() 0.015时发生的反应是:2NaAlO2+ CO2+3H2O=2Al(OH)3↓+Na2CO3。下列对应关系正确的是
0.015时发生的反应是:2NaAlO2+ CO2+3H2O=2Al(OH)3↓+Na2CO3。下列对应关系正确的是
选项 | n(CO2)/mol | 溶液中离子的物质的量浓度 |
A | 0 | c(Na+)>c(AlO2-)+c(OH-) |
B | 0.01 | c(Na+)>c(AlO2-)>c(OH-)>c(CO32-) |
C | 0.015 | c(Na+)>c(HCO3-)>c(CO32-)> c(OH-) |
D | 0.03 | c(Na+)>c(HCO3-)> c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制的流程。
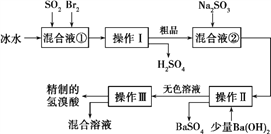
根据上述流程回答下列问题:
(1)混合液①中发生反应的化学方程式为________________________。
(2)溴与氯结合形成BrCl,BrCl的性质与卤素单质相似。则BrCl与水发生反应的化学方程式为___________________。
(3)加入Ba(OH)2反应的离子方程式为______________操作Ⅱ的名称是______。操作Ⅲ一般适用于分离______混合物。(选填编号)
a.固体和液体 b.固体和固体 c.互不相溶的液体 d.互溶的液体
(4)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)常带有淡淡的黄色。于是甲、乙两同学设计了简单实验加以探究:甲同学假设工业氢溴酸呈淡黄色是因为含有F![]() ,则用于证明该假设所用的试剂为______,反应的离子方程式为_____________。
,则用于证明该假设所用的试剂为______,反应的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期元素在周期表中的位置关系如图:

I.若Y元素原子的最外层电子数是电子层数的3倍
(1) W的原子结构示意图为___________________ 。
(2)Z在周期表中的位置 ____________________。
(3)一定条件下,X的最低价氢化物与X的某种氧化物按2:3物质的量比混合恰好反应生成X 单质和水,该氧化物的化学式为_____________。
(4)写出铜片置于Z的最高价氧化物水化物稀溶液,没有明显变化。加热,依然如故。再通入空气,溶液就逐渐变蓝,使溶液变蓝的反应的离子方程式:_______。
Ⅱ.若Y和Z的核外电子数之和为20。
(5)相对分子质量为16的Y的氢化物电子式为_______________________。
(6)写出单质Y和浓硝酸反应的化学方程式:________________________。
(7)写出工业制备Z的过程中发生的第一个反应的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),设起始
CO(g)+3H2(g),设起始![]() =Z,在恒压下,平衡时
=Z,在恒压下,平衡时![]() (CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
(CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是

A.该反应的焓变ΔH>0
B.图中Z的大小为a>3>b
C.图中X点对应的平衡混合物中![]() =3
=3
D.温度不变时,图中X点对应的平衡在加压后![]() (CH4)减小
(CH4)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色透明的强碱性溶液中,能大量共存的离子组是
A. Na+、K+、SO42-、HCO3- B. Cu2+、K+、SO42-、NO3-
C. Na2+、K+、Cl-、SO42- D. NH4+、K+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是同周期的短周期元素,原子序数依次增大。Y为地壳中含量最高的金属元素,Z是所在周期中非金属最强的元素,X、Y的最高价氧化物对应的水化物可以相互反应。
(1)Y元素的原子结构示意图是_________________。
(2)X、Z最高价氧化物对应的水化物之间发生反应的离子方程式为______________。
(3)Z、碳和氟三种元素可组成氟利昂(CZ3F),它在紫外线作用下破坏臭氧层的反应过程部如下:
①CZ3F![]() CZ2F·+Z·
CZ2F·+Z·
②Z·+O3![]() O2+ZO·
O2+ZO·
③ ZO·+O·![]() Z·+O2
Z·+O2
反应①中破坏的化学键属于________(填“极性”或“非极性”)共价键。
(4)下列说法正确的是___________(填字母)。
a.X与氧元素可形成碱性氧化物
b.常温下与水反应的难易程度可证明金属性:X>Y
c.X、Y、Z形成的简单离子的核外电子排布均相同
(5)Y、石墨与含YCl4-的离子液体可构成原电池,其工作原理如图所示。若电路中转移电子的物质的量为4. 5 mol,则消耗Y单质的质量是________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com