
| A£® | ŹŹĮæŃĪĖį | B£® | ŹŹĮæNaOH | C£® | ŹŹĮæNaHCO3 | D£® | ŹŹĮæKOH |
·ÖĪö Na2CO3ČÜŅŗÖŠ£¬ÓÉÓŚCO32-µÄĖ®½ā£¬Ź¹µĆc£ØCO32-¼õŠ”£¬Čē¹ūŅŖNa2CO3ČÜŅŗÖŠ$\frac{c£ØN{a}^{+}£©}{c£ØC{{O}_{3}}^{2-}£©}$µÄ±ČÖµ±äŠ”£¬ŌņŠčŅŖŅÖÖĘĢ¼ĖįøłĄė×ÓĖ®½ā£¬øł¾ŻĖ®½āĘ½ŗāµÄŅʶÆÓ°ĻģŅņĖŲĄ“»Ų“š
½ā“š ½ā£ŗA”¢¼ÓČėŃĪĖį£¬ŃĪĖįÓėCO32-·“Ó¦£¬»įŹ¹µĆĢ¼ĖįøłĄė×ÓÅØ¶Č¼õŠ”£¬ČÜŅŗÖŠ$\frac{c£ØN{a}^{+}£©}{c£ØC{{O}_{3}}^{2-}£©}$µÄ±ČÖµ±ä“󣬹ŹA“ķĪó£»
B”¢¼ÓNaOHČÜŅŗ£¬ČÜŅŗÖŠc£ØNa+£©Ōö“ó£¬C£ØCO32-£©¼õŠ”£¬ČÜŅŗÖŠ$\frac{c£ØN{a}^{+}£©}{c£ØC{{O}_{3}}^{2-}£©}$µÄ±ČÖµ±ä“󣬹ŹB“ķĪó£»
C”¢¼ÓNaOH ¹ĢĢ壬ČÜŅŗÖŠc£ØNa+£©Ōö“ó£¬ČÜŅŗÖŠ$\frac{c£ØN{a}^{+}£©}{c£ØC{{O}_{3}}^{2-}£©}$µÄ±ČÖµ±ä“󣬹ŹC“ķĪó£»
D”¢¼ÓČėĒāŃõ»Æ¼Ų¹ĢĢ壬»įŅÖÖĘĢ¼ĖįøłĖ®½ā£¬¼ÓČėĖ®Ļ”ŹĶ»įµ¼ÖĀČÜŅŗÖŠĄė×ÓÅØ¶Č¼õŠ”£¬ČÜŅŗÖŠ$\frac{c£ØN{a}^{+}£©}{c£ØC{{O}_{3}}^{2-}£©}$µÄ±ČÖµ±äŠ”£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éѧɜŃĪµÄĖ®½āĘ½ŗāµÄÓ°ĻģŅņĖŲÖŖŹ¶£¬×¢ŅāÖŖŹ¶µÄŹįĄķŗĶ¹éÄÉŹĒ½āĢāµÄ¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū | B£® | ¢Ū¢Ś¢Ł | C£® | ¢Ś¢Ū¢Ł | D£® | ¢Ł¢Ū¢Ś |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
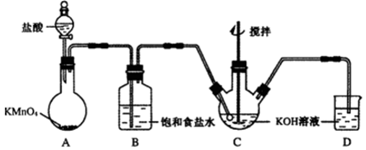
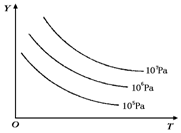 ÓŠĻĀĮŠæÉÄę·“Ó¦£ŗL£Øs£©+G£Øg£©?2R£Øg£©£ØÕż·“Ó¦ĪüČČ£©£¬Ķā½ēĪĀ¶Č”¢Ń¹ĒæµÄ±ä»Æ¶ŌøĆ·“Ó¦µÄÓ°ĻģČēĶ¼ĖłŹ¾£ŗŌņĻĀĮŠ¶ŌĶ¼ÖŠ×Ż×ų±źYµÄŗ¬ŅåµÄÓŠ¹ŲŠšŹöÖŠÕżČ·µÄŹĒ£Ø””””£©
ÓŠĻĀĮŠæÉÄę·“Ó¦£ŗL£Øs£©+G£Øg£©?2R£Øg£©£ØÕż·“Ó¦ĪüČČ£©£¬Ķā½ēĪĀ¶Č”¢Ń¹ĒæµÄ±ä»Æ¶ŌøĆ·“Ó¦µÄÓ°ĻģČēĶ¼ĖłŹ¾£ŗŌņĻĀĮŠ¶ŌĶ¼ÖŠ×Ż×ų±źYµÄŗ¬ŅåµÄÓŠ¹ŲŠšŹöÖŠÕżČ·µÄŹĒ£Ø””””£©| A£® | GµÄ×Ŗ»ÆĀŹ | B£® | Ę½ŗā»ģŗĻĘųÖŠRµÄĢå»ż·ÖŹż | ||
| C£® | Ę½ŗā»ģŗĻĘųÖŠGµÄĢå»ż·ÖŹż | D£® | Ę½ŗā»ģŗĻĘųÖŠLµÄĢå»ż·ÖŹż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 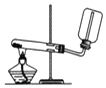 ŹµŃéŹŅÖĘČ”²¢ŹÕ¼ÆNH3 | B£® | 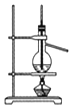 ŹÆÓĶµÄÕōĮó | ||
| C£® | 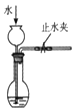 ¼ģ²é×°ÖĆĘųĆÜŠŌ | D£® | 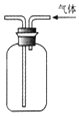 ĄūÓĆÅÅæÕĘų·¢ŹÕ¼ÆCO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | FeCl3ČÜŅŗŹ¹Ą¶É«ŹÆČļŹŌÖ½±äŗģ£ŗFe3++3H2OØT3H++Fe£ØOH£©3 | |
| B£® | FeCl3ČÜŅŗÖŠµĪ¼Ó°±Ė®³öĻÖŗģŗÖÉ«³Įµķ£ŗFe3++3OH-ØTFe£ØOH£©3”ż | |
| C£® | ÓĆFeCl3ČÜŅŗøÆŹ“Ó”Ė¢µēĀ·°å£ŗFe3++CuØTCu2++Fe2+ | |
| D£® | ¼ģŃéČÜŅŗÖŠµÄFe3+ÓĆKSCNČÜŅŗ£ŗFe3++3SCN-?Fe£ØSCN£©3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com