
 ��
��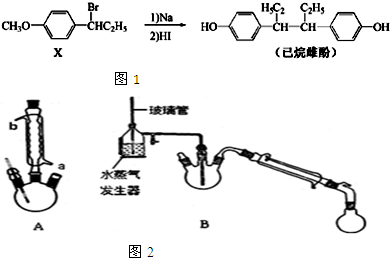
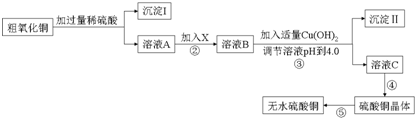
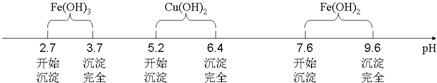
���� ��1�����ݲ�����������Ч�����жϣ�
��2������ʵ��ԭ����֪��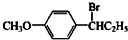 ���Ƶ�������������
���Ƶ������������� ��
�� ��������������HI��Ӧ����
��������������HI��Ӧ����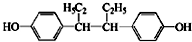 ���ݴ˴��⣻
���ݴ˴��⣻
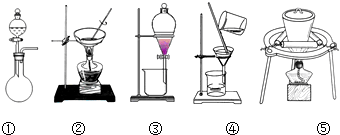
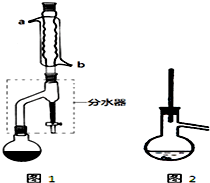
��3������װ��ͼ��֪�������ܿ���ƽ����ѹ�����װ���Ƿ�������
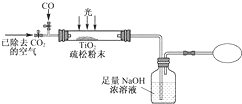
��4��X�������������ˮ�����Ե��۲쵽װ��B���������� Һ���Ϊ��ɫ����˵��ˮ�������������X�Ѿ���ȥ��
��5����ʵ����ҪĿ�����ᴿ����Ʒӣ��÷�Ӧ��ȡ�ķ������Ƚ�����Ʒ������Ҵ�������ˮ��ȥ�Ҵ������˿ɵ����ղ�Ʒ��
��� �⣺��1�����ݲ�����������Ч���ÿ�֪����������aͨ������ˮ��
�ʴ�Ϊ��a��
��2������ʵ��ԭ����֪�� ���Ƶ�������������
���Ƶ������������� ��
�� ��������������HI��Ӧ����
��������������HI��Ӧ����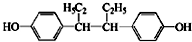 �����Բ�����з�Ӧ�Ļ�ѧ����ʽΪ
�����Բ�����з�Ӧ�Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��3������װ��ͼ��֪�������ܿ���ƽ����ѹ�����װ���Ƿ�������
�ʴ�Ϊ��ƽ����ѹ�����װ���Ƿ�������
��4��X�������������ˮ�����Ե��۲쵽װ��B���������� Һ���Ϊ��ɫ����˵��ˮ�������������X�Ѿ���ȥ��
�ʴ�Ϊ��Һ���Ϊ��ɫ����
��5����ʵ����ҪĿ�����ᴿ����Ʒӣ��÷�Ӧ��ȡ�ķ������Ƚ�����Ʒ������Ҵ�������ˮ��ȥ�Ҵ������˿ɵ����ղ�Ʒ������ʵ���˳��Ϊdbca��
�ʴ�Ϊ��dbca��
���� ���⿼��������롢�ᴿʵ��ķ�������ƣ�Ϊ��Ƶ���㣬�������ʵ����ʼ�ʵ������Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬��Ŀ�Ѷ��еȣ�


 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2p1��p2 | B�� | PCl5�ķֽ������� | ||
| C�� | p1��p2 | D�� | Cl2������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | ��������/mL | п������/g | п����״ | �¶�/�� | ��ȫ�������ʱ��/s | ��������п������/g |
| �� | 50.0 | 2.0 | ��Ƭ | 15 | 200 | m1 |
| �� | 50.0 | 2.0 | ��Ƭ | 25 | 100 | m2 |
| �� | 50.0 | 2.0 | ���� | 25 | 70 | m3 |
| �� | 50.0 | 2.0 | ���� | 35 | 35 | m4 |
| �� | 50.0 | 2.0 | ��ĩ | 25 | t1 | 5.0 |
| �� | 50.0 | 4.0 | ��ĩ | 25 | t2 | m5 |
| �� | 50.0 | 6.0 | ��ĩ | 25 | t3 | 14.9 |
| �� | 50.0 | 8.0 | ��ĩ | 25 | t4 | 19.3 |
| �� | 50.0 | 10.0 | ��ĩ | 25 | t5 | m6 |
| �� | 50.0 | 12.0 | ��ĩ | 25 | t6 | 19.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �ζ����� | ��һ�� | �ڶ��� | ������ |
| �ζ�ǰ������mL�� | 0.10 | 0.36 | 1.10 |
| ���������mL�� | 20.12 | 20.34 | 22.12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 �л���ķ�Ӧ�������渱��Ӧ��������� ��Ҫ�����ᴿ����һ��ˮ���㾫�ĺϳɲ������£�
�л���ķ�Ӧ�������渱��Ӧ��������� ��Ҫ�����ᴿ����һ��ˮ���㾫�ĺϳɲ������£�| ������ | ������ | ������ | ���������� | ������ |
| �ܶ�/��g/mL�� | 0.810 | 1.049 | 0.882 | 0.7689 |
| �е�/�� | 117.8 | 118.1 | 126.1 | 143 |
| ��ˮ�е��ܽ��� | ���� | ���� | ���� | ���� |
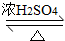 CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
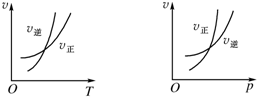 ���淴ӦmA��g��?nB��g��+pC��g����H=Q���¶Ⱥ�ѹǿ�ı仯�������淴Ӧ���ʵ�Ӱ��ֱ������ͼ�е�����ͼ������������ȷ���ǣ�������
���淴ӦmA��g��?nB��g��+pC��g����H=Q���¶Ⱥ�ѹǿ�ı仯�������淴Ӧ���ʵ�Ӱ��ֱ������ͼ�е�����ͼ������������ȷ���ǣ�������| A�� | m��n+p��Q��0 | B�� | m��n+p��Q��0 | C�� | m��n+p��Q��0 | D�� | m��n+p��Q��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �¶�/�� | 700 | 830 | 1200 |
| Kֵ | 1.7 | 1.0 | 0.4 |
| A�� | ��Ӧ��ʼ��ƽ�⣬A��ƽ����Ӧ����v��A��=0.005 mol•L-1•s-1 | |
| B�� | ����ѹǿ�������淴Ӧ���ʾ��ӿ� | |
| C�� | �÷�Ӧ����Ϊ���ȷ�Ӧ�������¶ȣ�Kֵ����ƽ�������ƶ� | |
| D�� | �ﵽƽ���B��ת����Ϊ50% |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com