
设NA为阿伏伽德罗常数,下列说法正确的是
A. 1L1mol/L的盐酸溶液中,所含HCl分子数为NA
B. 常温常压下,71gCl2溶于水,转移的电子数目为0.1NA
C. 标准状况下,22.4LSO2和SO3的混合物,含硫原子的数目为NA
D. 0.5mol乙醇中含有的极性共价键数目为3.5NA
科目:高中化学 来源:2016-2017学年江苏省扬州市宝应县高二下学期学业水平测试(三)化学试卷(解析版) 题型:选择题
下列过程吸收热量的是
A. 氧化钙与水反应 B. 氮气液化 C. 碳酸钙分解 D. 浓硫酸稀释
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省洛阳市高二(平行班)3月月考化学试卷(解析版) 题型:填空题
A、B、C、D、E、F为原子序数依次增大的六种元素,A的一种同位素可用于考古测定生物的死亡年代,C原子的最外层电子数是次外层的3倍,D与B同主族;E的原子序数是A、B之和的2倍;F的原子序数为29。回答下列问题:
(1)六种元素中第一电离能最大的是 (填元素符号),其中D原子价电子排布图为 。
(2)基态E原子核外未成对电子数为 。
(3)BC2-的立体构型为 ,与其互为等电子体的分子是 (写化学式)。
(4)FC在加热条件下容易转化为F2C,从原子结构的角度解释原因 ;F晶体的堆积方式为 (填序号)。
①简单立方堆积 ②体心立方堆枳 ③六方最密堆积 ④面心立方最密堆积
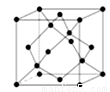
(5)硼与D可形成一种耐磨材料G,其结构与金刚石相似(如图),可由硼的三溴化物和D的三溴化物高温下在氢气的氛围中合成。G的晶胞边长为a Pm,则该晶体密度的表达式为 g· cm﹣3(含a、NA的式子表示,不必化简)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省洛阳市高二(平行班)3月月考化学试卷(解析版) 题型:选择题
关于化学键的各种叙述中,下列说法中正确的是( )
A. 含有金属元素的化合物一定是离子化合物
B. 共价化合物里,一定不存在离子键
C. 由多种非金属元素组成的化合物一定是共价化合物
D. 由不同种元素组成的多原子分子里,一定只存在极性键
查看答案和解析>>
科目:高中化学 来源:2017届陕西省西安市高三模拟(一)理综化学试卷(解析版) 题型:选择题
电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。在一定温度下,用0.1mol/LKOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的盐酸和醋酸溶液,滴定曲线如图所示。下列有关判断正确的是
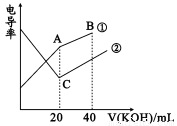
A. B点的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+)
B. A点的溶液中有:c(CH3COO-)+c(OH-)-c(H+)=0.1mol/L
C. C点水电离的c(OH-)大于A点水电离的c(OH-)
D. A、B、C三点溶液均有Kw=c(H+)·c(OH-)=1.0×10-14
查看答案和解析>>
科目:高中化学 来源:2017届天津市高三第四次月考化学试卷(解析版) 题型:简答题
A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)B在周期表中的位置为第______周期第_______族。
(2)E元素形成的氧化物对应的水化物的化学式为______。
(3)元素B、C、D、E形成的简单离子半径大小关系是_________。(用离子符号表示)。
(4)用电子式表示化合物D2C的形成过程:_________。
(5)由A、B、C三种元素形成的离子化合物的化学式为_________,它与强碱溶液共热,发生反应的离子方程式是_________。
(6) D2EC3一定条件下可以发生分解反应生成两种盐,其中一种产物为无氧酸盐,则此反应的化学方程式为
_________。(化学式用具体的元素符号表示)。
(7)E的某种氧化物是大气污染物之一,也是某工业生产中的主要尾气之一。某校兴趣小组欲采用下列方案测定此工业尾气中的E的氧化物的含量。
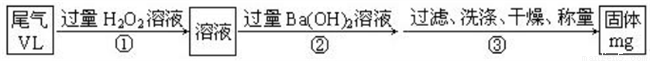 通过的尾气体积为VL(已换算成标准状况)时,该尾气中E的氧化物含量(体积分数)为_______(用含有V、m的代数式表示).
通过的尾气体积为VL(已换算成标准状况)时,该尾气中E的氧化物含量(体积分数)为_______(用含有V、m的代数式表示).
查看答案和解析>>
科目:高中化学 来源:2017届江苏省苏州市高三上学期期末考试化学试卷(解析版) 题型:填空题
苏州工匠用白铜打造的食蟹工具“蟹八件”,主要成分是铜镍合金。Ni能与CO形成正四面体形的配合物Ni(CO)4,CuSO4溶于氨水形成[Cu(NH3)4]SO4深蓝色溶液。
(1)Cu基态原子核外电子排布式为________________。
(2)1 mol Ni(CO)4中含有σ键的数目为_______________。
(3)[Cu(NH3)4]SO4中阴离子的空间构型是___________,与SO42-互为等电子体的分子为_______________。(填化学式)
(4) NH3的沸点_______________。(选填“高于”或“低于”)PH3,原因是_______________。
(5)某白铜合金晶胞结构如右图所示.晶胞中铜原子与镍原子的个数比为_______________。
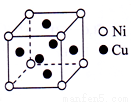
查看答案和解析>>
科目:高中化学 来源:2017届江苏省苏州市高三上学期期末考试化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、W的原子序数依次增大。X、W在同一主族,Z+与Y3-具有相同的电子层结构,X原子的最外层电子数是其内层电子数的2倍。下列说法不正确的是
A. X的气态简单氢化物的热稳定性比W的强
B. 由Y、Z两种元素组成的化合物是离子化合物
C. W的氧化物可与Z的最高氧化物对应水化物反应
D. 粒子半径的大小顺序:r(W)>r(X)>r(Z+)>r(Y3-)
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三3月高考模拟化学试卷(解析版) 题型:选择题
下列离子组能以较大浓度共存的是( )
A. 含有0.1mol·L-1Fe3+的溶液中:K+、Mg2+、I-、NO3-
B. 使酚酞试液变红的溶液:Na+、Cl-、SO42-、CO32-
C. 含有0.1mol·L-1Ca2+的溶液中:Na+、K+、CO32-、Cl-
D. 碳酸氢钠溶液:K+、SO42-、Cl-、H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com