
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:
| 1 |
| 11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、凡能导电的物质一定是单质 |
| B、金属单质都能与稀硫酸发生置换反应 |
| C、活泼金属都能从盐溶液中置换出较不活泼的金属 |
| D、在化学反应中,金属单质失电子,常作还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
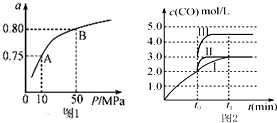 甲醇是主要的化学工业基础原料和清洁液体燃料.工业上可以用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
甲醇是主要的化学工业基础原料和清洁液体燃料.工业上可以用CO或CO2来生产燃料甲醇.已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:| 化学反应及平衡常数 | 温度/℃ | ||
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g)△H1 | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?CO(g)+H2O(g)△H2 | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g)△H3 | K3 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、需要加热才能发生的反应一定是吸热反应 |
| B、吸热反应在不加热的条件下一定不能发生 |
| C、吸热反应的反应物的总能量之和小于生成物的总能量之和 |
| D、某可逆反应,若正反应为吸热反应,逆反应也可能是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氮气是还原产物,二氧化碳是氧化产物 |
| B、HNCO中碳元素被氧化 |
| C、1molHNCO参加反应失去3mol电子 |
| D、氧化产物与还原产物质量比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同温同压下,28g的CO与N2组成的混合气体中含有原子数一定为2NA |
| B、0.1mol?L-1的稀硫酸中含有SO42-个数为0.1NA |
| C、56克铁在氯气中完全燃烧,共转移3NA个电子 |
| D、1L 1mol/L 的盐酸中含有NA个HCl分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | CH3COOH溶液的体积/mL | NaOH溶液的体积/mL | 结论 |
| ① | 0 | 20.00 | NaOH溶液pH=13 |
| ② | x | 20.00 | 反应后溶液呈碱性 |
| ③ | y | 20.00 | 反应后溶液呈中性 |
| A、NaOH溶液的浓度等于0.01mol.L-1 |
| B、CH3COOH溶液的浓度可能等于2/x mol.L-1 |
| C、CH3COOH溶液的浓度等于2/y mol.L-1 |
| D、②组反应后混合液中,离子浓度相对大小关系为:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com