
镓(Ga)、锗(Ge)、砷(As)、硒(Se)均为第四周期的元素,它们在高科技尖端
科学特别是信息领域有着广泛的用途。试回答下列问题:
(1)基态锗原子的价电子排布式为_________________________________。
(2)沸点:NH3________AsH3(填“>”、“<”或“=”,原因是______________
____________________________________________________________________.
(3)某砷的氧化物俗称“砒霜”,其分子结构如右图所示,该化合物的分子式
为_______________,As原子采取__________________杂化。
(4) H2SeO4和H2SeO3是硒的两种含氧酸,请根据结构与性质的关系,解释H2SeO4比H2SeO3酸性强的原因_________________________________________________ 。
(5)砷化镓可由(CH3)2Ga和AsH3在700℃下反应制得,反应的方程式
为_________________;砷化镓的晶胞结构如下图所示,其晶胞边长为a pm,
则每立方厘米该晶体中所含砷元素的质量为____________g(用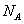 表示阿伏
表示阿伏
 加德罗常数的值)。
加德罗常数的值)。

科目:高中化学 来源: 题型:
下列有关仪器刻度位置的叙述正确的是
A.容量瓶容积的刻度线刻在瓶颈上
B.滴定管的“0”标线刻在管的下端
C.托盘天平游码刻度尺的“0”标线刻在尺的右边
D.量筒的最下端刻“0”标线
查看答案和解析>>
科目:高中化学 来源: 题型:
制备食用碘盐(KIO3)原理之一为: ,下列说法正确的是
,下列说法正确的是
A.向KClO3溶液中滴加AgNO3溶液得到白色AgCl沉淀
B.反应过程中I2置换出Cl2,由此可推断非金属性I> CI
C.KClO3和KIO3均属于离子化合物,都只含有离子键
D.制备KIO3的反应中氯元素被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关含铜化合物的说法错误的是(设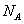 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
A.用盐酸可以洗去铜表面的铜锈
B. 0.1mol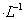 的CuSO4溶液中,Cu2+的数目一定小于0.1
的CuSO4溶液中,Cu2+的数目一定小于0.1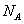
C.在CuCl2和FeCl3的混合溶液中加入铁粉,若有固体残留,则其中一定含有铜
D.在FeSO4溶液中加入CuS固体,溶液中c(Fe2+)不变,说明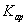 (CuS)远小于
(CuS)远小于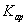 (FeS)
(FeS)
查看答案和解析>>
科目:高中化学 来源: 题型:
α鸢尾酮香料的分子结构如图所示,下列说法中不正确的是
A.α鸢尾酮可与某种酚互为同分异构体
B.1 mol α鸢尾酮最多可与3 mol H2加成
C.α鸢尾酮能发生银镜反应
D.α鸢尾酮经加氢→消去→加氢可转变为


查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A. 若反应X + Y = M是放热反应,该反应一定不用加热。
B. 需要加热方能发生的反应一定是吸热反应。
C. CO2与CaO化合是放热反应,则CaCO3分解是吸热反应。
D. 1mol硫酸与足量氢氧化钠发生中和反应生成水所释放的热量称为中和热。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学研究的正确说法是
A.同时改变两个变量来研究反应速率的变化,能更快得出有关规律
B.对于同一个化学反应,无论是正反应还是逆反应,其反应的焓变相同
C.根据11-17号元素最高价氧化物对应水化物的酸碱性递变规律,推出同周期元素的金属性、
非金属性递变规律
D.从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属递增的规律
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com