
| A. | 0.20 | B. | 0.25 | C. | 0.30 | D. | 0.35 |
分析 甲烷1.6即0.1mol和氧气8.0g即0.25mol燃烧反应完全后,得到二氧化碳和水,根据方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O,结合m=nM来计算.
解答 解:甲烷1.6即0.1mol和氧气8.0g即0.25mol燃烧反应完全后,根据方程式:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O得到二氧化碳0.1mol和水0.2mol,还剩余氧气0.05mol,则容器中所含的分子总物质的量为0.1mol+0.2mol+0.05mol=0.35mol,故选D.
点评 本题考查物质的量计算,比较基础,侧重对基础知识的巩固.


科目:高中化学 来源: 题型:选择题
| A. | Q1+Q2<2Q3 | B. | Q1+Q2>2Q3 | C. | Q1+Q2<Q3 | D. | Q1+Q2>Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 如果5.6LN2含有n个氮分子,则NA一定约为4n | |
| B. | 18g水中所含的电子数是8NA | |
| C. | 在0.5mol/L的氯化钡溶液中含有离子数为1.5NA | |
| D. | 15gCH3+含有8mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入BaCl2溶液产生不溶于稀HNO3的白色沉淀,说明原溶液中有SO42- | |
| B. | 加入盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO32-存在 | |
| C. | 验证烧碱溶液中是否含有Cl-,先加稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含Cl- | |
| D. | 加入NaOH溶液有白色沉淀出现,则原溶液中一定含有Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol H+含有的电子数 | |
| B. | 标准状况下,22.4L酒精所含的分子数 | |
| C. | 1.6 g CH4 含有的质子数 | |
| D. | 1L 1mol/L的硫酸钠溶液所含的Na+ 数 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | P-P键的键能大于P-Cl键的键能 | |
| B. | 可求Cl2(g)+PCl3(g)═PCl5(s)的反应热△H | |
| C. | Cl-Cl键的键能$\frac{b-a+5.6c}{4}$ kJ•mol-1 | |
| D. | 1molP4含4molp-p键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
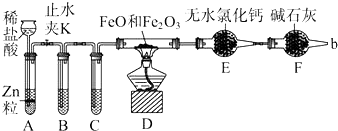
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com