
| A. | 18g≤m≤128g | B. | 36g<m<180g | C. | 18g<m<128g | D. | 36g<m≤180g |
分析 在一定温度下,某固态物质在100g溶剂中达到饱和状态时所溶解的溶质的质量,叫做这种物质在这种溶剂中的溶解度;根据溶解度的定义并运用极限法计算,分两种情况分析:一种是:正好形成了CuSO4.5H2O晶体,另一种是:正好形成饱和溶液.
解答 解:用极限法解答.
a.假设正好形成了CuSO4.5H2O晶体,则$\frac{32}{m}$=$\frac{160}{90}$,m=18g;
b.假设正好形成饱和溶液,则溶质质量为32g,溶剂质量为mg,故$\frac{32}{m}$=$\frac{25}{100}$,m=128,由于形成饱和CuSO4溶液并有CuSO4•5H2O晶体析出,故m的取值范围为18g<m<128g,
故选C.
点评 本题考查范围讨论题的计算,为高频考点,侧重考查学生分析计算能力,根据混合物形成物质成分及特点采用极限法分析解答,题目难度中等.


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:解答题
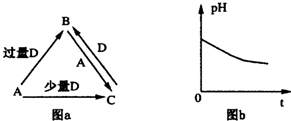
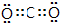 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 需鉴别物质 | 方法1 | 方法2 | |
| A | 硫酸铵和磷矿粉 | 加水溶解 | 加熟石灰 |
| B | 一氧化碳和二氧化碳 | 闻气味 | 通过灼热的氧化铜 |
| C | 食盐水和蒸馏水 | 测pH | 蒸发结晶 |
| D | 真黄金和假黄金 (铜铝合金) | 看颜色 | 灼烧 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
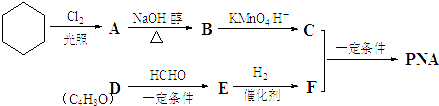
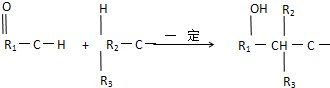 (R1、R2、R3代表烃基
(R1、R2、R3代表烃基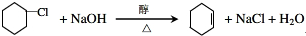 .
. .
.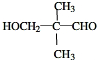 .
. .
.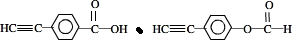 .
.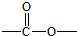 基团
基团查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com