
 金片上剪下一小块(质量为1.0g),立即投入到盛有10mL10mol/LNaOH溶液的小烧杯中。
金片上剪下一小块(质量为1.0g),立即投入到盛有10mL10mol/LNaOH溶液的小烧杯中。 极反应式:
极反应式:  每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:不详 题型:单选题
| A.NaAlO2 | B.NaAlO2和NaOH | C.Al(OH)3 | D.NaOH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
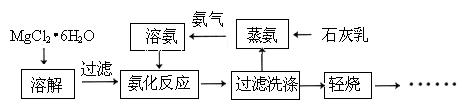 |
| A.MgO | B.NaOH | C.Mg(OH)2 | D.KSCN |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 NaOH溶液至沉淀质量不再变化,用去350mLNaOH溶液。则所取样品中铝的物质的量为( )
NaOH溶液至沉淀质量不再变化,用去350mLNaOH溶液。则所取样品中铝的物质的量为( )查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | 浓盐酸 | 浓硫酸 | 浓硝酸 | 浓氢氧化钠溶液 |
| 铝 | 实验1 | 实验2 | 实验3 | 实验4 |
| 铁 | 实验5 | 实验6 | 实验7 | 实验8 |
| 铜 | 实验9 | 实验1O | 实验11 | 实验12 |
 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2.7g | B.4.6g | C.8.2g | D.无法计算 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com