
 ��2013?�㶫ģ�⣩����ʯ��һ�ֺ�ˮ�ĸ�þ�����ο�����ܳƣ����Կ�����MgO��Fe2O3��Al2O3��SiO2��ɣ�ʵ����������ʯΪԭ����ȡˮ�ϼ�ʽ̼��þ����֪��
��2013?�㶫ģ�⣩����ʯ��һ�ֺ�ˮ�ĸ�þ�����ο�����ܳƣ����Կ�����MgO��Fe2O3��Al2O3��SiO2��ɣ�ʵ����������ʯΪԭ����ȡˮ�ϼ�ʽ̼��þ����֪��| �������� | Fe��OH��3 | Al��OH��3 | Mg��OH��2 |
| ��ʼ������pH | 1.5 | 3.3 | 9.4 |
| ��ȫ������pH | 3.7 | 5.2 | 11.0 |


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ���� | Fe��OH��2 | Fe��OH��3 | Zn��OH��2 | Cu��OH��2 |
| KSP | 8.0��10-16 | 4.0��10-38 | 3.0��10-17 | 2.2��10-20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
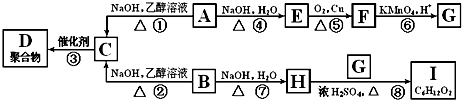




| ŨH2SO4 |
| �� |
| ŨH2SO4 |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


| ˮ |
| ˮ |

 +CH3CH2Cl
+CH3CH2Cl +HCl
+HCl +CH3CH2Cl
+CH3CH2Cl +HCl
+HCl

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com