
NO2、CO、CO2是对环境影响较大的气体,对它们的合理控制、利用是优化我们生存环境的有效途径。
(1)如图所示,利用电化学原理将NO2 转化为重要化工原料C。
若A为NO2,B为O2,则负极的电极反应式为___________;

(2)光气 (COCl2)是一种重要的化工原料,用于农药、医药、
聚酯类材料的生产,工业上通过
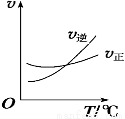
Cl2(g)+CO(g)  COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:
COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:
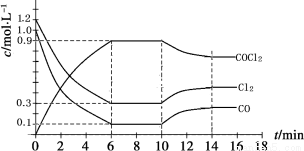
0~6 min内,反应的平均速率v(Cl2)= ;
保持温度不变,在第7min 向体系中加入这三种物质各2mol,则平衡向____________ 方向移动(填“正反应”、“逆反应”或“不”);
将初始投料浓度变为c(Cl2)=0.7mol/L、c(CO)=0.5mol/L、c(COCl2)=______ mol/L,
保持反应温度不变,则最终达到化学平衡时,Cl2的体积分数与上述第6min时Cl2的体积分数相同;
温度升高,该反应平衡常数变化的趋势是______;(填“增大”、“减小”或“不变”)
比较第8min反应温度T(8)与第15min反应温度T(15)的高低:T(8)_____T(15)
(填“<”、“>”或“=”)
 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源:2015-2016学年青海省高一下期末化学试卷(解析版) 题型:选择题
元素的性质随着元素原子序数的递增而呈周期性变化的原因是( )
A. 元素原子的核外电子排布呈周期性变化
B. 元素的原子半径呈周期性变化
C. 元素的化合价呈周期性变化
D. 元素的金属性、非金属性呈周期性变化
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第二次周测化学试卷(解析版) 题型:选择题
常温下,现有浓度都为0.1mol·L-1HX、HY的溶液各20ml,分别用0.1 mol·L-1NaOH溶液滴定。溶液的pH与加入NaOH溶液体积V的关系如图所示。

下列判断错误的是
A.滴定过程中,水电离的c(H+)·c(OH-)均不变
B.HX的电离程度小于HY的电离程度
C.V=10ml时,c(HX)+c(X-)=2c(Na+)
D.V=20ml时,c(Y-)>c(X-)
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期第一次月考理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】
根据已学物质结构与性质的有关知识,回答下列问题:
(1)请写出第三周期元素中p轨道上有3个未成对电子的元素符号:____________,某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4,该元素的名称是____________。
(2)根据价层电子对互斥理论推测下列离子或分子的空间立体构型:H3O+____________,BF3____________。
(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解,得到深蓝色的透明溶液,写出有关化学反应方程式____________、_________。
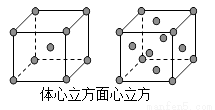
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。则体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为____________;若两种晶体中最邻近的铁原子间距离相同,则体心立方晶胞和面心立方晶胞的密度之比为_______。
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期第一次月考理综化学试卷(解析版) 题型:选择题
下列各溶液中分别加入Na2O2固体,充分反应后既有无色气体又有白色沉淀产生的是
A.(NH4)2SO4溶液 B.MgCl2溶液
C.NaHCO3溶液 D.CuSO4溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春第十一中高一下期末考化学(解析版) 题型:选择题
在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验 编号 | 温度/℃[ | 起始时物质的量/mol | 平衡时物质的量/mol[来] | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.40 | 0.10 | 0.090 |
② | 800 | 0.10 | 0.40 | 0.080 |
③ | 800 | 0.20 | 0.30 | a |
④ | 900 | 0.10 | 0.15 | b |
下列说法正确的是( )
A.实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速率v(N)=2.0×10-2mol/(L·min)
B.实验②中,该反应的平衡常数K=2.0
C.实验③中,达到平衡是,X的转化率为60%
D.实验④中,达到平衡时,b>0.060
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春第十一中高一下期末考化学(解析版) 题型:选择题
已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示。下列说法正确的是( )
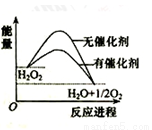
A.加入催化剂,减小了反应的热效应
B.加入催化剂,可提高H2O2的平衡转化率
C.H2O2分解的热化学方程式:2H2O2 = 2H2O + O2 ΔH>0
D.反应物的总能量高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春第十一中高一下期末考化学(解析版) 题型:选择题
在2L密闭容器中发生反应N2+3H2?2NH3,经一段时间后NH3的物质的量增加了2.4mol,这段时间内用氢气表示的反应速率为0.6mol/(L.s),则这段时间为( )
A.6s B.4s C.3s D.2s
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省揭阳市高二期末统考理综化学试卷(解析版) 题型:填空题
氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸。工业上采用如下工艺流程,从某酸性废液(主要含Cu2+、Fe3+、 H+、Cl-)中制备氯化亚铜。
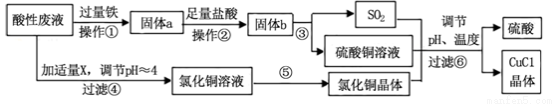
请回答下列问题:
(1)写出步骤①中发生的两个主要反应的离子方程式: 。
(2)步骤②的操作名称是: 。
(3)步骤④中所加物质X为: 。
(4)步骤⑤的操作是: 。
(5)步骤⑥应调节溶液pH呈酸性,且用乙醇洗涤CuCl晶体,目的是: 。
(6)在CuCl的生成过程中,可以循环利用的物质是 ,理论上 (填“是”或“不”)需要补充(不考虑调节等消耗);理由是 。
(7)工业上还可以采用以碳棒为电极电解CuCl2溶液得到CuCl。电解CuCl2溶液,阴极上发生的电极反应式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com