
���� ��1������Һ�м��������BaCl2��Һ���а�ɫ�������������ˣ���SO42-��CO32-�е�һ�ֻ��У���һ��û��Ba2+��
��2������1������Һ�����AgNO3��Һ���а�ɫ������������ɫ����ΪAgCl�������������ӣ�����ȷ���Ƿ�Cl-��
��3������1���еij�������ϡ�����У�����������ʧ���������������һ����SO42-��CO32-����û��H+����ϵ���غ���
��� �⣺��1������Һ�м��������BaCl2��Һ���а�ɫ�������������ˣ���SO42-��CO32-�е�һ�ֻ��У���һ��û��Ba2+��
��2������1������Һ�����AgNO3��Һ���а�ɫ������������ɫ����ΪAgCl�������������ӣ�����ȷ��ԭ��Һ���Ƿ�Cl-��
��3������1���еij�������ϡ�����У�����������ʧ���������������һ����SO42-��CO32-����û��H+������Һ���Ե��ԣ���һ����Na+��
����������һ����SO42-��CO32-��Na+��һ��û��H+��Ba2+�����ܺ���Cl-��
��1��ԭ��Һ��һ������SO42-��CO32-��Na+���ʴ�Ϊ��SO42-��CO32-��Na+��
��2��һ��û��H+��Ba2+���ʴ�Ϊ��H+��Ba2+��
��3�����ܺ���Cl-����Ҫȷ���������Ƿ���ڣ�Ӧ�����ų��������̼����ĸ��ţ���ԭ��Һ�м������ᱵ��ȥ�����̼��������˺�����Һ�м���ϡ�����ữ��Һ��Ȼ���ټ��������������а�ɫ�������ɣ���֤��ԭ��Һ�к��������ӣ��ʴ�Ϊ��Cl-��ABC��
��4��̼�ᱵ��ϡ���ᷴӦ�����Ȼ����Ͷ�����̼���壬���ӷ�Ӧ����ʽΪ��BaCO3+2H+�TBa2++H2O+CO2�����ʴ�Ϊ��BaCO3+2H+�TBa2++H2O+CO2����
���� ���⿼�����ӵĹ��棬Ϊ��Ƶ���㣬���ճ����ijɷּ���������֮��ķ�ӦΪ���Ĺؼ������ظ��ֽⷴӦ�����ӹ��濼�飬��Ŀ�ѶȲ���


 ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д�
ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д� ���������ν�ϵ�д�
���������ν�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Na2CO3������CO2�� | B�� | NaHCO3������CO2�� | ||
| C�� | NaHCO3�ķ�Ӧ���ʿ� | D�� | ���߲���CO2һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ķ���ϩ�Ļ�ѧ��Ժ�ǿ | B�� | ���ķ���ϩ�����к���˫�� | ||
| C�� | ���ķ���ϩ�ĵ����Dz������� | D�� | ���ķ���ϩ�з�������������76% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
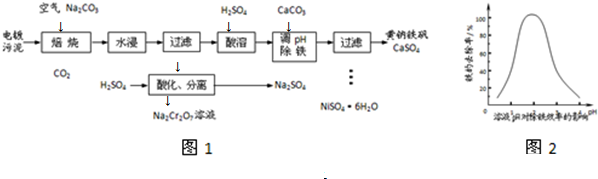
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
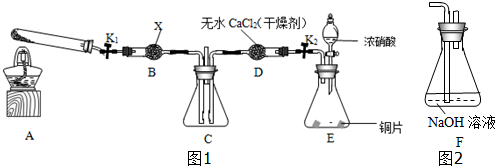
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͭ$\stackrel{Ũ����}{��}$����ͭ | B�� | ͭ$\stackrel{ϡ����}{��}$����ͭ | ||
| C�� | Cu$\stackrel{Cl_{2}}{��}$CuCl2$\stackrel{AgNO_{3}}{��}$Cu��NO3��2 | D�� | Cu$\stackrel{����}{��}$CuO$\stackrel{HNO_{3}}{��}$Cu��NO3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��� | �¶ȣ��棩 | ��ʼ���ʵ��� ��mol�� | ƽ�����ʵ��� ��mol�� | �ﵽƽ������ʱ�� ��s�� | |
| PCl5��g�� | PCl3��g�� | Cl2��g�� | |||
| �� | 320 | 0.40 | 0.10 | 0.10 | t1 |
| �� | 320 | 0.80 | t2 | ||
| �� | 410 | 0.40 | 0.15 | 0.15 | t3 |
| A�� | ƽ�ⳣ��K�������������� | |
| B�� | ��Ӧ����ƽ��ʱ��PCl5��ת���ʣ������������� | |
| C�� | ��Ӧ����ƽ��ʱ������I�е�ƽ������Ϊv��PCl5��=$\frac{0.10}{{t}_{1}}$mol/��L•s�� | |
| D�� | ��ʼʱ���������г���PCl5 0.30 mol��PCl30.45 mol��Cl20.10 mol����Ӧ�����淴Ӧ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| t/s | 0 | 50 | 150 | 250 | 350 |
| n��B��/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A�� | ǰ50 s��B��ƽ����Ӧ����v��B��=0.0032 mol•L-1•s-1 | |
| B�� | ��ͬ�¶��£����ﵽƽ����������м�������A����ƽ�������ƶ���ƽ�ⳣ������ | |
| C�� | ��ͬ�¶��£�����ʼʱ�������г���1.0 mol A��0.20 mol B��0.20 mol C����ﵽƽ��ǰv��������v���棩 | |
| D�� | �����������������䣬�����¶ȣ�ƽ��ʱ��ƽ�ⳣ��K=0.2 mol•L-1����Ӧ�ġ�H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �¶ȡ�������䣬������� | B�� | �������䣬����ϵ���� | ||
| C�� | �¶ȡ�������䣬�������� | D�� | �¶Ȳ��䣬����������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com