
【题目】I. 雾霾严重影响人们的生活,汽车尾气排放是造成雾霾天气的重要原因之一。已知汽车尾气排放时容易发生以下反应:
①N2(g)+O2(g)![]() 2NO(g) ΔH1=a kJ·mol-1
2NO(g) ΔH1=a kJ·mol-1
②2NO(g)+O2(g)![]() 2NO2(g) ΔH2=b kJ·mol-1
2NO2(g) ΔH2=b kJ·mol-1
③CO(g)+![]() O2(g)
O2(g)![]() CO2(g) ΔH3=c kJ·mol-1
CO2(g) ΔH3=c kJ·mol-1
④2CO(g)+2NO(g)![]() N2(g)+2CO2(g) ΔH4
N2(g)+2CO2(g) ΔH4
(1)根据反应①②③,确定反应④中ΔH4=___________ kJ·mol-1。
II. 如图是一个化学过程的示意图,请回答下列问题:
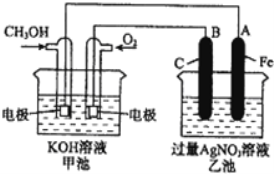
(2)请回答图中甲、乙两池的名称.乙池是_______________装置。
(3)通入甲醇的电极的电极反应式为_________________________________。
(4)乙池中反应的化学方程式为_____________________________________。
(5)电解一段时间后,乙池中A(Fe)极的质量增加5.4g时,且溶液的体积为500mL,求所得溶液在25℃时的pH=__________ ,甲池中消耗O2为 __________mL(标准状况下)。
【答案】2c-a 电解池 CH3OH - 6e﹣+ 8OH﹣ = CO32﹣ + 6H2O 4AgNO3 + 2H2O ![]() 4Ag + O2↑ + 4HNO3 1 280
4Ag + O2↑ + 4HNO3 1 280
【解析】
I.(1)利用盖斯定律计算反应④的ΔH4;
II.甲池是甲醇燃料电池,通入甲醇的电极是负极、通入氧气的电极是正极;乙池是电解池,电极B与正极相连,B是阳极,电极A与负极相连,A是阴极。
(1)①N2(g)+O2(g)![]() 2NO(g) ΔH1=a kJ·mol-1
2NO(g) ΔH1=a kJ·mol-1
③CO(g)+![]() O2(g)
O2(g)![]() CO2(g) ΔH3=c kJ·mol-1
CO2(g) ΔH3=c kJ·mol-1
根据盖斯定律,③×2-①得④2CO(g)+2NO(g)![]() N2(g)+2CO2(g) ΔH4=2c-a;
N2(g)+2CO2(g) ΔH4=2c-a;
(2)乙池与燃料电池甲相连,乙池是电解装置。
(3)甲池是甲醇燃料电池,通入甲醇的电极是负极,甲醇失电子生成碳酸钾,电极反应式为CH3OH - 6e﹣+ 8OH﹣ = CO32﹣ + 6H2O。
(4)乙池是电解池,用惰性电极电解硝酸银溶液,反应的化学方程式为4AgNO3 + 2H2O ![]() 4Ag + O2↑ + 4HNO3。
4Ag + O2↑ + 4HNO3。
(5)电解一段时间后,乙池中A(Fe)极的质量增加5.4g,即生成5.4g Ag,Ag的物质的量是![]() ,电路中转移0.05mol电子,根据
,电路中转移0.05mol电子,根据![]() ,乙池生成硝酸的物质的量是0.05mol,乙池溶液的体积为500mL,氢离子浓度为0.1mol/L,在25℃时的pH=1,甲池中消耗O2为
,乙池生成硝酸的物质的量是0.05mol,乙池溶液的体积为500mL,氢离子浓度为0.1mol/L,在25℃时的pH=1,甲池中消耗O2为![]() 280mL(标准状况下)。
280mL(标准状况下)。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是
A.含16g氧原子的二氧化硅晶体中含有的键数目为1NA
B.1 mol N2与4 mol H2反应生成的NH3分子数为2NA
C.50℃时,1.0 L pH=1的H2SO4 溶液中含有的H+数目为0.1NA
D.12 g石墨烯(单层石墨)中含有六元环的数目为1.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年5月千年繁华的古城扬州开通了宁启动车,标志着古城扬州正式迈入“动车时代”,动车铁路在建设施工中要大量使用各种材料.
①生产水泥和玻璃都用到的原料是______;制备玻璃的反应方程式______![]() 任写一个
任写一个![]() .
.
②动车车厢内饰板材多采用![]() 聚碳酸酯
聚碳酸酯![]() 及PC合金板材,PC属于______
及PC合金板材,PC属于______![]() 填字母
填字母![]() .
.
![]() 金属材料
金属材料![]() 无机非金属材料
无机非金属材料![]() 有机高分子材料
有机高分子材料
③动车大量使用铝合金材料制作车厢.下列有关铝合金叙述正确的是______![]() 填字母
填字母![]() .
.
![]() 属于纯净物
属于纯净物![]() 密度小,硬度大
密度小,硬度大![]() 在空气中易被腐蚀
在空气中易被腐蚀
④铁路建设中如何防止铁轨的腐蚀是工程技术人员攻克的难题之一.铁在发生电化学腐蚀时的负极反应方程式为______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用微生物燃料电池原理,可以处理宇航员排出的粪便,同时得到电能。美国宇航局设计的方案是:用微生物中的芽孢杆菌来处理粪便产生氨气,氨气与氧气分别通入燃料电池两极,最终生成常见的无毒物质。示意图如下所示。下列说法错误的是( )
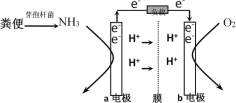
A.a电极是负极,b电极是正极
B.负极区发生的反应是2NH3 - 6e-=N2+6H+
C.正极区,每消耗标准状况下2.24 L O2,a向b电极转移0.4 mol电子
D.电池工作时电子通过由a经负载流向b电极,再穿过离子交换膜回到a电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示(部分物质和条件已略去)。A是海水中含量最多的盐,B是最常见的无色液体,E、F、G常温下均为气体,F呈黄绿色,G是最简单的烃,F与G按物质的量之比1∶1反应生成I和J,H是一种既能溶于I溶液又能溶于D溶液的白色固体,C由两种短周期元素组成,其摩尔质量为144 g·mol-1。

请回答下列问题:
(1)I的电子式为______。
(2)C的化学式为______。
(3)写出反应①的化学方程式_______。
(4)写出反应②的离子方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)25℃时,pH=5的CH3COOH溶液中,由水电离出的氢离子浓度c(H+)=______
molL﹣1;往溶液中加入少量NaOH固体,则溶液中![]() _____(填“增大”、“减小”或“不变”),写出表示该混合溶液中所有离子浓度之间的一个等式:______。
_____(填“增大”、“减小”或“不变”),写出表示该混合溶液中所有离子浓度之间的一个等式:______。
(2)甲醇(CH3OH)是一种可再生能源,具有广阔的开发和应用前景。以甲醇、氧气和KOH溶液为原料,石墨为电极制造新型手机电池,甲醇在_____极反应(填“正”或“负”),电极反应式为_____。
(3)泡沫灭火器的原理:________________________(用离子反应方程式表示)。
(4)Na2CO3溶液中所有离子的大小关系是:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应热的说法正确的是 ( )
A.化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关
B.已知C(s)+![]() O2(g)=CO(g)的反应热为110.5kJ/mol,说明碳的燃烧热为110.5kJ
O2(g)=CO(g)的反应热为110.5kJ/mol,说明碳的燃烧热为110.5kJ
C.反应热的大小与反应物所具有的能量和生成物所具有的能量无关
D.当H为“-”时,表示该反应为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液分别加到HA、HB两种弱酸溶液中,两溶液中pH与粒子浓度比值的对数关系如图所示,已知![]() ,下列有关叙述错误的是( )
,下列有关叙述错误的是( )
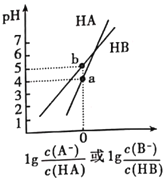
A.HA、HB两种酸中,HB的酸性弱于HA
B.b点时,![]()
C.同浓度同体积的NaA和NaB溶液中,阴离子总数相等
D.向HB溶液中加入NaOH溶液所得的混合溶液中,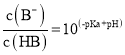
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】充分燃烧2.8g某有机物A,生成8.8g CO2和3.6g H2O,这种有机物蒸气的相对密度是相同条件下N2的2倍。
(1)求该有机物的分子式。
(2)该有机物链状同分异构体的结构简式为: 。
(3)若在核磁共振氢谱中只有一个信号峰(即只有一种氢原子),则用键线式表示的结构简式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com