
碘在科研与生活中有重要应用,某兴趣小组用0.50 mol·L-1 KI、0.2%淀粉溶液、0.20 mol·L-1 K2S2O8、0.10 mol·L-1 Na2S2O3等试剂,探究反应条件对化学反应速率的影响。
已知:S2O82-+2I- 2SO42-+I2(慢) I2+2S2O32-
2SO42-+I2(慢) I2+2S2O32- 2I-+ S4O62-(快)
2I-+ S4O62-(快)
向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的 耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32-与S2O82-初始的物质的量需满足的关系为:n(S2O32-)∶n(S2O82-) 。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验序号 | 体积V/mL | ||||
K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
表中Vx mL,理由是 。
(3)已知某条件下,浓度c(S2O82-)反应时间t的变化曲线如图所示,若保持其他条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82-)-t的变化曲线示意图(进行相应的标注)

碘也可用作心脏起搏器电源-锂碘电池的材料,该电池反应为: 2Li(s)+I2(s) 2LiI(s)ΔH
2LiI(s)ΔH
已知: ①4Li(s)+O2(g) 2Li2O(s) ΔH1 ②4LiI(s)+O2(g)
2Li2O(s) ΔH1 ②4LiI(s)+O2(g) 2I2(s)+2Li2O(s)ΔH2
2I2(s)+2Li2O(s)ΔH2
则电池反应的ΔH= ;碘电极作为该电池的 极。
(1)Na2S2O3 < 2
(2)2.0 保证反应物K2S2O8浓度改变,而其它的条件不变,才能达到实验目的
(3)
(4) ,正
,正
【解析】
试题分析:(1)由反应的离子方程式可以看出当反应I2+2S2O32-=2I-+ S4O62-不再发生时容器内含有一定量的I2,溶液颜色将由无色变为蓝色。即当Na2S2O3耗尽时溶液颜色将由无色变为蓝色。根据两个反应方程式中的物质的关系可知:n(S2O32-)∶n(S2O82-)<2,才可以有I2存在,也才能确保能观察到蓝色。(2)要探究反应物浓度对化学反应速率的影响,其它条件都相同,变量为K2S2O8溶液的浓度,根据①②可知混合溶液的体积为10ml.所以③中取K2S2O8 8.0ml,则需要水的体积为2.0ml.(3)降低温度,化学反应速率减慢,达到平衡所需要的时间延长;加入催化剂,化学反应速率加快。达到平衡所需要的时间缩短。c(S2O82-)与时间的关系见答案。(4)(①-②)÷2可得2Li(s)+I2(s)=2LiI(s)ΔH= 。由于在反应中Li失去电子,作负极。而碘得到电子,因此碘电极作为该电池的正极。
。由于在反应中Li失去电子,作负极。而碘得到电子,因此碘电极作为该电池的正极。
考点:考查滴定终点时溶液中物质的量的关系、浓度、温度、催化剂对化学反应速率的影响及原电池反应原理的知识。


科目:高中化学 来源:2015届江苏省淮安市协作体高二下学期期中考试化学试卷(解析版) 题型:填空题
mA(气) + nB(气) pC(气) + qD(气)的 C %与时间 t有如图关系
pC(气) + qD(气)的 C %与时间 t有如图关系
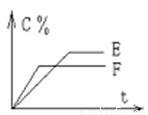
(1)若E、F表示两种温度,则 E____F(填“>”、“<”或“=”),正反应____ 热。
(2)若E、F表示两种压强,则 m + n_____p + q。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省沭阳县高二下学期期中调研测试化学试卷(解析版) 题型:选择题
铜锌原电池(如右图)工作时,下列叙述正确的是

A.在外电路中,电流从Zn极流向Cu极
B.盐桥中的Cl-移向CuSO4溶液
C.当负极减小65g时,正极增加65g
D.电池的总反应为 Zn + Cu2+=Zn2+ + Cu
查看答案和解析>>
科目:高中化学 来源:2015届江苏省无锡江阴市高二下学期期中考试化学试卷(解析版) 题型:选择题
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应平均速率为0.6 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.15mol·L-1·s-1
③2s时物质A的转化率为30%
④2s时物质B的浓度为0.3 mol·L-1
其中正确的是
A.①③ B.①④ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源:2015届江苏省无锡江阴市高二下学期期中考试化学试卷(解析版) 题型:选择题
下列过程一定不能自发进行的是:
A.2N2O5(g)=4NO2(g)+O2(g);ΔH>0
B.2CO(g)=2C(s)+O2(g);ΔH>0
C.(NH4)2CO3(s)=NH4HCO3(s)+NH3(g);ΔH>0
D.2H2(g)+O2(g)=2H2O(l);ΔH<0
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高二下学期4月阶段测试化学试卷(解析版) 题型:选择题
在体积为2 L的恒容密闭容器中发生反应xA(g)+yB(g) zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是

A.200℃时,反应从开始到平衡的平均速率v(B)= 0. 02 mol·L-1·min-1
B.图Ⅱ所知反应xA(g)+yB(g) zC(g)的△H<0,且a=2
zC(g)的△H<0,且a=2
C.若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前v(正)>v(逆)
D.200℃时,向容器中充入2 mol A 和1 mol B,达到平衡时,A 的体积分数小于0.5
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高二下学期4月阶段测试化学试卷(解析版) 题型:选择题
下列说法不正确的是

A.NH3·H2O NH4++OH-达到平衡后,升高温度平衡正向移动
NH4++OH-达到平衡后,升高温度平衡正向移动
B.在海轮的外壳上镶入锌块,可减缓船体的腐蚀速率
C.明矾水解生成Al(OH)3胶体,可用作净水剂
D.如图所示的反应过程中A+B→X的△H<0,X→C的△H>0
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三上学期摸底考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.反应CaCO3(s)=CaO(s)+CO2(g)在常温下不能发生,则该反应的△H>0
B.0.1 mol·L-1CH3COOH溶液加水稀释后,溶液中 的值减小
的值减小
C.铅蓄电池在放电过程中,负极质量增加,正极质量减少
D.锅炉中沉积的CaSO4可用饱和Na2CO3溶液浸泡,再将不溶物用稀盐酸溶解除
查看答案和解析>>
科目:高中化学 来源:2015届广西桂林市高三上学期第一次月考化学试卷(解析版) 题型:选择题
标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为w,物质的量浓度为c mol·L-1,则下列关系中不正确的是
A、w=17c/(1 000ρ) B、w=17V/(17V+22 400)
C、c=1 000Vρ/(17V+22 400) D、ρ=(17V+22 400)/(22.4+22.4V)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com