
【题目】下列关于分子式为C4H8O2的有机物的同分异构的说法中不正确的是
A. 属于酯类的有4种 B. 既含有羟基又含有醛基的有3种
C. 存在分子中含有六元环的同分异构体 D. 属于羧酸类的有2种
【答案】B
【解析】A、C4H8O2属于酯类的同分异构体,为饱和一元酯,若为甲酸与丙醇形成的酯,甲酸只有1种结构,丙醇有2种,形成的酯有2种,若为乙酸与乙醇形成的酯,乙酸只有1种结构,乙醇只有1种结构,形成的乙酸乙酯有1种,若为丙酸与甲醇形成的酯,丙酸只有1种结构,甲醇只有1种结构,形成的丙酸甲酯只有1种,所以C4H8O2属于酯类的同分异构体共有4种,A正确;B、C4H8O2属于羟基醛时,可以是2-羟基丁醛、3-羟基丁醛、4-羟基丁醛、2-甲基-2-羟基丙醛、2-甲基-3羟基丙醛,共5种同分异构体,B错误;C、存在分子中含有六元环的同分异构体: ,C正确;D、C4H8O2属于羧酸时,可以是丁酸或2-甲基丙酸,共有2种同分异构体,D正确;答案选B。
,C正确;D、C4H8O2属于羧酸时,可以是丁酸或2-甲基丙酸,共有2种同分异构体,D正确;答案选B。


科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]秸秆(含多糖类物质)的综合应用具有重要的意义。下面是以秸秆为原料合成聚酯类高分子化合物的路线:

回答下列问题:
(1)下列关于糖类的说法正确的是______________。(填标号)
a.糖类都有甜味,具有CnH2mOm的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为______。
(3)D中官能团名称为______,D生成E的反应类型为______。
(4)F 的化学名称是______,由F生成G的化学方程式为______。
(5)具有一种官能团的二取代芳香化合物W是E的同分异构体,0.5 mol W与足量碳酸氢钠溶液反应生成44 g CO2,W共有______种(不含立体结构),其中核磁共振氢谱为三组峰的结构简式为_________。
(6)参照上述合成路线,以(反,反)-2,4-己二烯和C2H4为原料(无机试剂任选),设计制备对二苯二甲酸的合成路线_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然有机化合物甲的结构简式如图3,该物质具有一定的除草功效,有关该化合物的说法正确的是( )
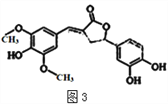
A. 既能与FeCl3发生显色反应,也能和NaHCO3反应放出CO2
B. 1 mol该化合物最多能与6 mol NaOH 反应
C. 1 mol 该化合物最多能与含5 mol Br2的浓溴水反应
D. 该化合物分子中含有三种含氧官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于碳酸(H2CO3)和硅酸(H2SiO3)的说法中不正确的是( )
A. 两者均为弱酸
B. 两者均可使紫色石蕊试液变红色
C. CO2气体通入Na2SiO3溶液中可以制得硅酸
D. 两者受热时均可以分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种光化学电池的结构如右图,当光照在表面涂有氯化银的银片上时,发生反应:AgCl(s) ![]() Ag(s)+Cl(AgCl), [Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着Cl(AgCl)+e-→Cl-(aq),若将光源移除,电池会立即回复至初始状态。下列说法正确的是
Ag(s)+Cl(AgCl), [Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着Cl(AgCl)+e-→Cl-(aq),若将光源移除,电池会立即回复至初始状态。下列说法正确的是

A. 光照时,电流由Y流向X
B. 光照时,当转移0.1mole-时在Pt电极上有0.05molCl2生成
C. 光照时,Cl-向Ag电极移动
D. 光照时,电池总反应为:AgCl(s) +Cu+(aq) ![]() Ag(s)+Cu2+(aq)+Cl-
Ag(s)+Cu2+(aq)+Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且有两种常见化合物DA2和DA3;工业上电解熔融C2A3制取单质C, B、E除最外层均只有2个电子外,其余各层全充满,E位于元素周期表的ds区。回答下列问题:
(l) B、C中第一电离能较大的是_________,基态D原子价电子的轨道表达式为_______
(2) DA2分子的VSEPR模型是________。H3A比H2D熔沸点高得多的原因是_________。
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6在加热时易升华,与过量的NaOH 溶液反应可生成Na[C(OH)4]
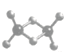
①C2Cl6属于_________晶体(填晶体类型),其中C原子的杂化轨道类型为______杂化。
②[C(OH)4]-中存在的化学健有__________。
(4)工业上制备B的单质是电解熔融B的氯化物,而不是电解BA,原因是_________。
(5)B、C的氯化物晶格能分别是2957KJ/mol、5492KJ/mol,二者相差很大的原因是________。
(6)D与E所形成化合物晶体的晶胞如右图所示。
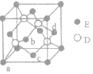
①在该晶胞中,E的配位数为__________。
②原子坐标参数可表示晶胞内部各原子的相对位置。右图晶胞中,原子坐标参数a为(0,0,0);b为(1/2,0,1/2),c为(1/2,1/2,0).则d原子的坐标为__________。
③已知该晶胞的密度为ρg/cm3,则其中两个D,原子之间的距离为____pm(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C1化学又称一碳化学,研究以含有一个碳原子的物质为原料合成工业产品的有机化学及工艺,因其在材料科学和开发清沽燃料方面的重要作用已发展成为一门学科。燃煤废气中的CO、CO2均能转化为基础化工原料、清洁能源甲醇:
①3H2(g)+CO2(g)![]() CH3OH(g) + H2O(l) △H1
CH3OH(g) + H2O(l) △H1
②CO(g)+2H2(g)![]() CH3OH(g) △H2
CH3OH(g) △H2
Ⅰ.已知:18g水蒸气变成液态水放出44KJ的热量。
化学键 | C-H | C-O | C=O | H-H | O-H |
键能/KJ/mol | 412 | 351 | 745 | 436 | 462 |
则△H1_____________________
Ⅱ.一定条件下,在恒容的密闭容器中投入1molCO 和2mol H2,反应②在催化剂作用下充分反应,CH3OH在平衡混合气中的体积分数在不同压强下随温度的变化如图l所示:
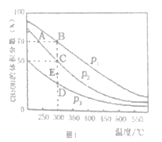
(1)图中压强的相对大小是P1______P2(填“>”“<”或“=”),判断的理由是________
(2)A、B、C三点的化学平衡常数的相对大小K(A)______K(B)_____ K(C)(填“>”“<”或“=”) ,计算C点的压强平衡常数Kp=__________(用平衡分压代替平衡浓度计算,分压=总压×体积分数)
(3)300℃,P2条件下,处于E点时V正________V逆(填“>”“<”或“=”)
(4)某温度下,不能说明该反应己经达到平衡状态的是______________。
a.容器内的密度不再变化
b. 速率之比v(CO):v(H2): v(CH3OH)=l: 2:l
c.容器内气体体积分数不再变化
d. 容器内混合气体的平均相对分子质量不再变化
e.容器内各组分的质量分数不再变化
(5)反应开始至在C点达平衡,各物质的浓度随时间变化曲线如图2所示,保持温度不变,t1时改变条件为_________,此时平衡_______。(填“正向移动”“逆向移动”“不移动” )
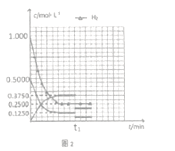
Ⅲ.工业上可通过甲醛羰基化法制取甲酸甲酯,25℃时,其反应的热化学方程式为:CH3OH(g)+CO(g) ![]() HCOOCH3(g),部分研究如下图所示:
HCOOCH3(g),部分研究如下图所示:
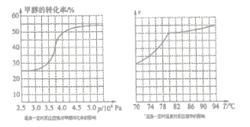
①根据反应体系的压强对甲醇转化率的影响并综合考虑生产成本因素的是_____(填下列序号字母)
a. 3.5×106Pa b. 4.0×106Pac. 5.0×106Pa
②用上述方法制取甲酸甲酯的实际工业生产中,采用的温度是80℃,其理由是_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向MgSO4、和A12(SO4)3的混合溶液中,逐滴加入NaOH溶液。下列图像中能正确表示上述反应的是(横坐标表示加入NaOH溶液的体积,纵坐标表示反应生成沉淀的质量)
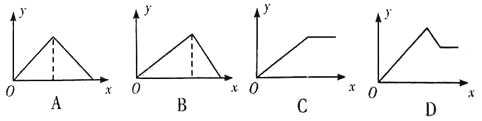
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类,填在横线上。
① ![]() __________; ②
__________; ② ![]() ___________;
___________;
③![]() ____________ ;④
____________ ;④![]() ;
;
⑤![]() ___________;
___________;
(2)某烃A 0.2 mol在氧气中充分燃烧后,生成化合物B、C各1 mol。
①烃A的分子式为 。
②若烃A不能使溴水褪色,但在一定条件下,能与Cl2发生取代反应,其一氯代物只有一种,则A的结构简式为 。
③若烃A能使溴水褪色,在催化剂作用下与H2加成,其加成产物分子中含有3个甲基,则A可能的结构简式为 ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com