
| A. | 臭氧空洞 | B. | 酸雨 | C. | 光化学烟雾 | D. | 温室效应 |
分析 A.制冷剂“氟里昂”等,对臭氧层有很大的破坏作用,会使臭氧层形成空洞;
B.酸雨是因为空气中的污染物二氧化硫、氮氧化合物等过多造成的;
C.光化学烟雾,是城市大气中的碳氢化合物(HC)和氮氧化合物(NOx)在阳光紫外线的作用下发生的一系列链式大气化学反应生成以臭氧(O3)为代表的刺激性二次污染物;
D.温室效应的主要气体二氧化碳,主要来自化石燃料的大量使用.
解答 解:A.制冷剂“氟里昂”等,对臭氧层有很大的破坏作用,会使臭氧层形成空洞,故A错误;
B.酸雨是因为空气中的污染物二氧化硫、氮氧化合物等过多造成的,故B正确;
C.大气中的碳氢化合物、氮氧化合物等为一次污染物,在太阳光中紫外线照射下能发生化学反应,衍生种种二次污染物.由一次污染物和二次污染物的混合物(气体和颗粒物)所形成的烟雾污染现象,称为光化学烟雾,故C错误;
D.造成温室效应的主要气体为二氧化碳,故D错误.
故选B.
点评 本题联系生活考查了环境污染和资源综合利用方面的知识,题目难度不大,同学们需要在平常生活中提高“节能、环保”的意识.


科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
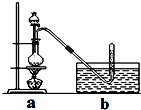
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
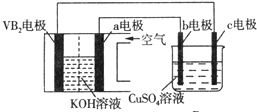
| A. | 电解过程中,c电极表面先有红色物质析出,后有气泡产生 | |
| B. | 外电路中电子由c电极流向VB2电极 | |
| C. | VB2电极发生的电极反应为:2VB2+11H2O-22e-═V2O5+2B2O3+22H+ | |
| D. | 若B装置内的液体体积为100 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
| 属于该类的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
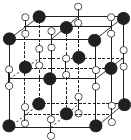 I.氮族元素和卤族元素都能形成许多种物质.
I.氮族元素和卤族元素都能形成许多种物质.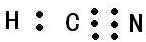 ;其中心C原子的杂化类型为sp.氮、磷、氟三种元素的电负性由大到小的顺序为F>N>P(用元素符号表示).
;其中心C原子的杂化类型为sp.氮、磷、氟三种元素的电负性由大到小的顺序为F>N>P(用元素符号表示).| F | Cl | Br | I | |
| 第一电力能(kJ•mol-1) | 1681 | 1251 | 1140 | 1008 |
| 晶体 | NaCl | KCl | CaO |
| 晶格能(kJ•mol-1) | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com