
已知由短周期元素组成的物质 A 、 B 、C 、D ,具有如下反应关系:
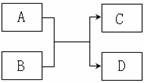 |
(1) 通常若A为黄绿色单质,B为无色液态化合物,且0.1mol/L的C溶液pH=1,则D物质的结构式为_____________
(2) 若B为化合物,且A、C两种无色气体相遇后变为红棕色,则B物质溶于水后显碱性的原因是__________________________________________________(用化学用语说明)
(3)若A为单质,C和D为常见的易燃气体,则该反应的化学方程式是____________________________________________________
(4) 若A为单质,B通常是无色液态化合物,灼烧D产生黄色火焰,则:
①若B分子含有10个电子,A与B反应的离子方程式是______________________________
②若B分子含有18个电子,则A+B→C+D的化学方程式为_____________________________
科目:高中化学 来源: 题型:
已知8 g A能与32 g B恰好完全反应,生成22 g C和一定量D,现将16 g A与70 g B的混合物充分反应后,生成2 mol D和一定量的C,则D的摩尔质量为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。
其中正确的是( )
| 选项 | 气体 | a | b | c | d |
| A | CO2 | 盐酸 | CaCO3 | 饱和Na2CO3 溶液 | 浓硫酸 |
| B | Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓硫酸 |
| C | NH3 | 饱和NH4Cl 溶液 | 消石灰 | H2O | 固体NaOH |
| D | NO | 稀硝酸 | 铜屑 | H2O | 浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是4mol/L和
2mol/L,取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的
气体的体积为(设反应中HNO3被还原成NO) ( )
A.0.448L B.0.224L C.0.896L D.0.672L
查看答案和解析>>
科目:高中化学 来源: 题型:
相同物质的量的下列物质:①金属钠 ②烧碱 ③过氧化钠 ④氧化钠,长期放置在空气中(不考虑潮解和水解),最后质量都会增加,按增加的质量由大到小排列,正确的是( )
A. ①>②>④>③ B. ①>②>③>④ C. ④>①>③>② D. ④>①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是
A.Fe3O4与稀硝酸反应:Fe3O4+8H+ = Fe2++2Fe3++4H2O
B.Na2S溶液呈碱性:S2-+H2O  HS-+OH-
HS-+OH-
C.用惰性电极电解饱和氯化钠溶液:2Cl-+2H+  H2↑+Cl2↑
H2↑+Cl2↑
D.Ca(HCO3)2与过量Ca(OH)2溶液反应: Ca2++2HCO3-+2OH- = CaCO3↓+CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
Ba(NO3)2可用于生产绿色烟花、绿色信号弹、炸药、陶瓷釉药等。钡盐生产中排出大量的钡泥[主要含有BaCO3、BaSO3、Ba (FeO2)2等],某主要生产BaCO3、BaSO4的化工厂利用钡泥制取Ba(NO3)2晶体(不含结晶水),其部分工艺流程如下:
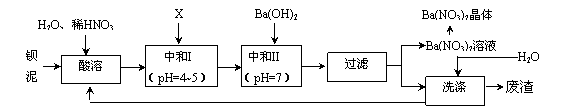
已知:①Fe3+和Fe2+以氢氧化物形式沉淀完全时,溶液的pH分别为3.2和9.7;
②Ba(NO3)2晶体的分解温度:592℃;
③kSP(BaSO4)=l.l×l 0-10,kSP (BaCO3)=5 .l×l0-9。
(1)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。试用离子方程式说明提纯原理_____________________________________________________________。
(2)上述流程中酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,反应的化学方程式为_______________________________________________。
(3)该厂结合实际,图中X应选用_____________(填字母)。
A.BaCl2 B.BaCO3 C.Ba(NO3) 2 D.Ba(OH) 2
(4)中和I使溶液的pH为4~5的目的是________________________________;结合离子方程式简述其原理:________________________________。
(5)从Ba(NO3)2溶液中获得其晶体的操作方法是_____________________。
(6)测定所得Ba(NO3)2晶体的纯度:准确称取wg晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量其质量为m g,则该晶体的纯度为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用脱脂棉包住约0.2 g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来。
(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:第一,有氧气生成;第二,________。过氧化钠跟水反应的化学方程式_______________________________________________________________。
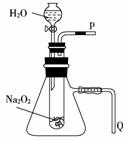
(2)某研究性学习小组拟用如图所示装置进行实验,以证明上述结论。用以验证第一条结论的实验方法及现象是__________________。
用以验证第二条结论的实验方法及现象是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有关甲醛(HCHO)、苯、二氧化碳及水说法不正确的是
|
| A. | 苯分子中所有原子共平面 |
|
| B. | 甲醛、苯和二氧化碳中碳原子均采用sp2杂化 |
|
| C. | 苯、二氧化碳是非极性分子,水和甲醛是极性分子 |
|
| D. | 水的沸点比甲醛高得多,是因为水分子间能形成氢键,而甲醛分子间不能形成氢键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com