
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
| A、新制的氯水可盛放在棕色细口瓶中 |
| B、水玻璃可存放在橡胶塞的细口瓶中 |
| C、配置FeCl3溶液,先加浓盐酸溶液溶解氯化铁固体,再稀释至相应浓度 |
| D、称取2.5g硫酸铜晶体,加100ml水溶液配制0.1mol.L-1硫酸铜溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | W | X | Y | Z |  |
| A | S | SO2 | SO3 | H2SO4 | |
| B | Na | Na2O2 | NaOH | NaCl | |
| C | Fe | FeCl3 | Fe(OH)2 | FeCl2 | |
| D | Al | AlCl3 | NaAlO2 | Al2(SO4)3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、NaHSO4溶液:c(Na+)+c(H+)=c(SO
| ||||
B、NH4Cl溶液:c(NH
| ||||
| C、20mL 0.1 mol?L-1 CH3COONa溶液与10mL 0.1mol?L-1HCl混合:c(Na+)>c(CH3COO-)>c(CH3COOH)>c(H+) | ||||
D、0.1mol?L-1 Na2C2O4溶液(H2C2O4)为二元弱酸):c(C2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol14CO2含有的中子数为22NA |
| B、1mol/LNH4NO3溶液中阴离子数为NA |
| C、标准状况下,22.4LCH3Cl含有的分子数为NA |
| D、2.7g铝与稀硫酸反应转移的电子数一定是0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
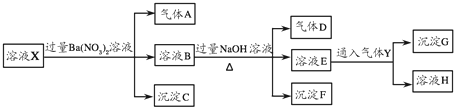
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe2(SO4)3溶液蒸干、灼烧,得到Fe2O3 |
| B、相同条件下,等物质的量浓度的溶液导电能力:NaOH>CH3COOH |
| C、溶液中结合质子(氢离子)的能力:CO32->HCO3->CH3COO- |
| D、海洋封存CO2会导致局部海洋水体酸性增强,会破坏海洋生态环境 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com