
(14��) 2013��10��9�գ�2013��ŵ������ѧ��������������̫���������ۻ�ѧ��������������˹������˹̹����ѧ��������ѧ�����˶�����ά�غ��ϼ��ݴ�ѧ��ѧ������Ү����л��������ӻ�ѧ��ϵ����˶�߶�ģ�Ͷ����������λ��ѧ�ҵ��о��ɹ��Ѿ�Ӧ���ڷ���������ֲ��Ĺ�����õ��о��У����������Ż�����������ҩ���̫���ܵ�ص���ơ�
����β����������Ҫԭ��Ϊ��2NO(g) + 2CO(g)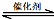 2CO2(g)+ N2(g) ��H��0
2CO2(g)+ N2(g) ��H��0
��1��ͬһ�����¸÷�Ӧ����Ӧ��ƽ�ⳣ��ΪK1���淴Ӧ�ı���ʽƽ�ⳣ��ΪK2��K1��K2�Ĺ�ϵʽ ��
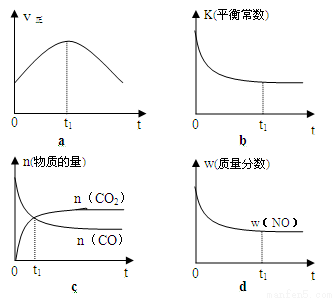
��2�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ�̴ﵽƽ��״̬���� ������ţ���
��3�������Ϊ10L���ܱ������У�����һ������CO2��H2����900��ʱ�������ȷ�Ӧ����¼ǰ5min�����ʵ�Ũ�ȣ���6min�ı��������������ʵ�Ũ�ȱ仯���±���
ʱ��/min | CO2��mol/L�� | H2��mol/L�� | CO��mol/L�� | H2O��mol/L�� |
0 | 0.2000 | 0.3000 | 0 | 0 |
2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
6 | 0.0350 | 0.1350 | 0.1650 |
��ǰ2min����CO��ʾ�ĸû�ѧ��Ӧ������Ϊ ��
�ڵ�5��6min��ƽ���ƶ��Ŀ���ԭ���� ��
��4��ֱ���ŷ�úȼ�ղ������������������صĻ������⡣úȼ�ղ����������������������CH4����ԭNOx�������������������Ⱦ��
��֪��CH4(g)+2NO2(g)��N2(g)��CO2(g)+2H2O(g) ��H����867 kJ/mol
2NO2(g)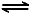 N2O4(g) ��H����56.9 kJ/mol
N2O4(g) ��H����56.9 kJ/mol
H2O(g) �� H2O(l) ��H����44.0 kJ��mol
д��CH4����ԭN2O4(g)����N2��H2O(l)���Ȼ�ѧ����ʽ�� ��
��5����һ�������£�������NH3����NOx����֪NO��NH3������Ӧ����N2��H2O������NO��NH3�Ļ����1mol����ַ�Ӧ��õ��Ļ�ԭ��������������1.4 g����ԭ��Ӧ�������NO�����ʵ���������_____________��
��6����һ�������£�Ҳ������H2���Դ���CO�ϳɼ״��Ͷ����ѣ�CH3OCH3���������������ʡ������������ʵ���1:1����Ӧ����ԭ�������ʴ�100%���ϳɵ����ʿ����� ��
a������ b���״� c����ȩ d������
��1��K1=K2-1
��2��bd
��3����0.0130mol/(L��min) �������¶Ȼ��СH2O��Ũ��
��4��CH4(g)+N2O4(g) ==N2(g) +2H2O(g) + CO2(g) ��H= ��898.1kJ/mol
��5��0.3mol��0.8mol
��6��c
��������
�����������1��2NO(g) + 2CO(g)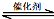 2CO2(g)+ N2(g) ��H��0��K1=
2CO2(g)+ N2(g) ��H��0��K1=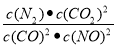 ���淴Ӧ��ƽ�ⳣ��K2=
���淴Ӧ��ƽ�ⳣ��K2=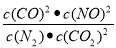 =
=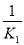 ������K1=K2-1 ��
������K1=K2-1 ��
��2�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У���Ӧ�ﵽƽ��״̬ʱ��Ũ�ȡ�ת���ʵȾ�����ʱ��ı仯���仯���ʣ���С��ѡ��bd��
��3����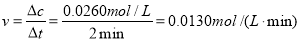 ;
;
�ڵ�5��6min��ƽ���ƶ���ԭ���������¶Ȼ��СH2O��Ũ�ȣ�
��4��CH4(g)+2NO2(g)��N2(g)��CO2(g)+2H2O(g) ��H����867 kJ/mol ��
2NO2(g)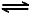 N2O4(g) ��H����56.9 kJ/mol ��
N2O4(g) ��H����56.9 kJ/mol ��
H2O(g) �� H2O(l) ��H �� ��44.0 kJ��mol ��
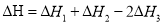 =-898kJ/mol
=-898kJ/mol
�Ȼ�ѧ����ʽΪCH4(g)+N2O4(g) ==N2(g) +2H2O(g) + CO2(g) ��H= ��898.1kJ/mol
��5��NO��NH3������Ӧ����N2��H2O����Ӧ����ʽΪ6NO+4NH3=5N2+6H2O����ַ�Ӧ��õ��Ļ�ԭ��������������1.4 g����ô��ԭ��������������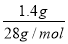 =0.05mol����Ϊ�������������NO��ȫ��Ӧ��n(NO)=
=0.05mol����Ϊ�������������NO��ȫ��Ӧ��n(NO)=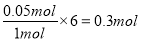 ������NH3��ȫ��Ӧ��n(NO)=
������NH3��ȫ��Ӧ��n(NO)=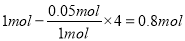 ��
��
��6�������������ʵ���1:1����Ӧ����ԭ�������ʴ�100%������ԭ���غ㣬��֪����Ϊ��ȩ����ѡ��C��
���㣺ƽ�ⳣ���ļ��㣬ƽ��״̬���жϣ���Ӧ���ʵļ��㣬�Ȼ�ѧ����ʽ����д����ѧ��Ӧ����ؼ���
��������� ����1����ѧ��Ӧ������ ����2����ѧ��Ӧ���� ����3����ѧƽ��״̬���ƶ� ��������

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015�Ĵ�ʡ�����и߶���ѧ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
������Ȳ��˵���������
A����Ȳ�ļ���Ϊ180�㣬�ǷǼ��Է���
B��̼ԭ��sp�ӻ�����γɦҼ���δ�ӻ�������2p����γ������м����һ��ഹֱ
C��̼̼������������������С��ͬ���������̼̼������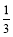
D����Ȳ�����м��м��Լ�Ҳ�зǼ��Լ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�걱����ʯ��ɽ������һģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͼ��ʾװ�ü����Ӧ����ʱ�����ܴﵽĿ�ĵ���
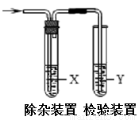
���ɵ����� | �Լ�X | �Լ�Y | |
A | ��ʯ��ˮ��Ӧ��ȡ����Ȳ | CuSO4��Һ | Br2��CCl4��Һ |
B | ľ̿��ŨH2SO4������ȡ�Ķ�����̼ | ����NaHCO3��Һ | ����ʯ��ˮ |
C | CH3CH2Br��NaOH�Ҵ���Һ������ȡ����ϩ | ˮ | KMnO4������Һ |
D | C2H5OH��ŨH2SO4������170����ȡ����ϩ | NaOH��Һ | Br2��CCl4��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ�����ڶ���ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
��15�֣�ij����ѧϰС���ͬѧ������ɰ��ȡ���Ტ�ⶨ������Ʒ�Ĵ��ȡ��Ʊ������ʵ���������£�
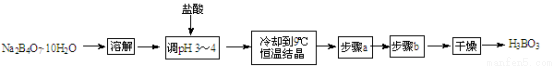
��1���ܽ���ɰʱ��Ҫ�IJ��������У��ձ���___________��
��2����pH��ֽ�ⶨ��ҺpH�IJ�������Ϊ__________________________________��
��3���������ữ��ɰ��Һ������������ӷ���ʽΪ_________________________��
��4��ʵ��������ȱ�ٵIJ���a������b�����ֱ�Ϊ_________��_________��
��5����������̫�������ü�ı���Һֱ�ӵζ���ʵ���ҳ����ü�ӵζ�������ԭ��Ϊ��
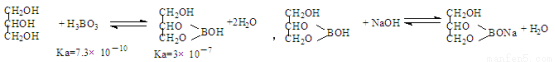
�������

�ٵζ����յ�ʱ��Һ��ɫ�仯��______________________________________��
�����ζ����յ�ʱ����NaOH����Һ22.00mL���εζ���õ�������Ʒ���������������Ϊ__________________���ٶ����ʲ���Ӧ����
�����ζ�ʱ�ζ��ܼ��첿�������ݣ��ζ���������ʧ�������²�õĽ��_____����ѡ���ƫ����ƫС�����䡱����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ�����ڶ���ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ����
A��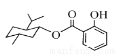 �ķ���ʽΪC17H24O3
�ķ���ʽΪC17H24O3
B���ṹΪ����CH=CH��CH=CH��CH=CH��CH=CH�����ĸ߷��ӻ�����䵥������Ȳ
C���л�����ѣ�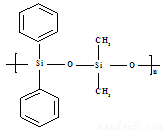 �����ɵ���
�����ɵ���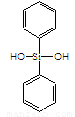 ��
�� ���۶���
���۶���
D���������ļ״�����ȩ��������ȫȼ��ʱ�ĺ��������ε���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�����и�����ѧ�ڵ�һ���¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й��ڷ���ʽΪC4H8O2���л����ͬ���칹���˵���У�����ȷ����
A�������������4��
B���������������2��
C�����ڷ����к�����Ԫ����ͬ���칹��
D���Ⱥ����ǻ��ֺ���ȩ������3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ������ѧ�ڳ��������ۻ�ѧ�Ծ��������棩 ���ͣ������
��Ԫ�صĻ�����Ӧ��ʮ�ֹ㷺����ش�
��1�����ȼ��Һ̬ƫ������(C2H8N2)����Һ̬N2O4�������������߷�Ӧ�ų��������ȣ�������������Ⱦ�������ˮ����֪�����£�1 gȼ����ȫȼ���ͷų�������Ϊ42.5 kJ����÷�Ӧ���Ȼ�ѧ����ʽΪ ��
��2��298 Kʱ����2 L�̶�������ܱ������У��������淴Ӧ��
2NO2(g) N2O4(g) ��H��-a kJ��mol��1(a��0)
N2O4(g) ��H��-a kJ��mol��1(a��0)
N2O4�����ʵ���Ũ����ʱ��仯��ͼ����ƽ��ʱ��N2O4��Ũ��ΪNO2��2�����ش��������⣺
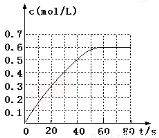
�� 298kʱ���÷�Ӧ��ƽ�ⳣ��Ϊ L��mol��1(��ȷ��0.01)��
������������Ǵ���ƽ��״̬���� ��
A.���������ܶȱ��ֲ��䣻
B.����������ɫ���ٱ仯��
C.��ѹ�㶨ʱ��
������Ӧ��398K���У�ijʱ�̲��n(NO2)=0.6 mol��n(N2O4)=1.2 mol�����ʱV(���� V(�棩(���������������=��)��
��3��NH4HSO4�ڷ����Լ���ҽҩ�����ӹ�ҵ����;�㷺��
����100 mL 0.1 mol��L��1 NH4HSO4��Һ�еμ�0.1 mol��L��1 NaOH��Һ���õ�����ҺpH��NaOH��Һ����Ĺ�ϵ������ͼ��ʾ���Է���ͼ��a��b��c��d��e����㣬
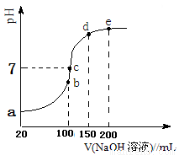
��b��ʱ����Һ�з���ˮ�ⷴӦ��������______��
����c�㣬��Һ�и�����Ũ���ɴ�С������˳�� ��
��d��e���Ӧ��Һ�У�ˮ����̶ȴ�С��ϵ��d e(���������������=��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ����������в����ظ�����ѧ�ڷ�У���п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ռ�ʵ���ҡ��칬һ�š��Ĺ���ϵͳ������������ȼ�ϵ��(RFC)��RFC��һ�ֽ�ˮ��⼼��������ȼ�ϵ�ؼ������ϵĿɳ���ء���ͼΪRFC����ԭ��ʾ��ͼ���й�˵����ȷ����
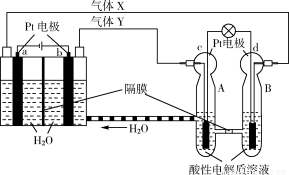
A��ת��0.1 mol����ʱ��a�缫����1.12 L H2
B��b�缫�Ϸ�����ԭ��Ӧ
C�����Ե������Һ��H������c�缫
D��d�缫�Ϸ����ĵ缫��Ӧ�ǣ�O2��4H����4e�� = 2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫ʡ��������ѧ����ɽһ�и����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�����ӷ���ʽ��ȷ����
A������������Һͨ�����CO2��Ca2+ + 2ClO- + H2O + CO2 = CaCO3�� + 2HClO
B������������Һͨ������SO2��Ca2+ + 2ClO- + H2O + SO2 = CaSO3�� + 2HClO
C��Ba(OH)2��Һ�������Al2(SO4)3��3Ba2++6OH��+2Al3++3SO42�� 3BaSO4��+2Al��OH��3��
D����Mg(HCO3)2��Һ�м����������ʯ��ˮ��Mg2++2HCO3��+2OHһ+Ca2+ MgCO3��+CaCO3��+2H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com