
| A. | 常温常压下,28g CO和N2的混合物含有的分子数为 NA | |
| B. | 标准状况下,1mol氦气中含有的核外电子数为4NA | |
| C. | 标准状况下,22.4 L 苯中含有的苯分子数是NA | |
| D. | 常温常压下,0.10 mol•L-1CH3COOH溶液中含有的H+数小于0.1NA |
分析 A.利用极值法依据n=$\frac{m}{M}$计算物质的量,分析判断分子数;
B.氦气是单原子分子;
C.气体摩尔体积使用对象为气体;
D.溶液体积未知.
解答 解:A.CO和N2的摩尔质量都为28g/mol,所以28g CO和N2的混合物物质的量为1mol,含有的分子数为 NA,故A正确;
B.标准状况下,1mol氦气中含有的核外电子数为2NA,故B错误;
C.标况下,苯为液体,不能使用气体摩尔体积,22.4 L 苯中含有的苯分子数大于NA,故C错误;
D.溶液体积未知,无法计算溶液中氢离子的个数,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的应用,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,注意气体摩尔体积使用条件和对象,题目难度不大.


科目:高中化学 来源: 题型:解答题
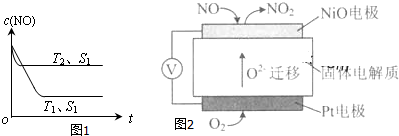
浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
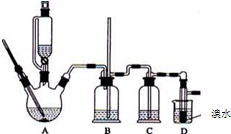 实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如下图所示:
实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如下图所示:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴离子具有氧化性 | B. | 溴离子的还原性比氯离子弱 | ||
| C. | 该反应属于复分解反应 | D. | 氯气的氧化性比溴单质强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素最高化合价:Al>Mg | B. | 金属性:Al>Mg | ||
| C. | 酸性:H2SO4>H3PO4 | D. | 原子半径:Cl>F |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 定容摇匀后,有少量溶液外流,则NaClO的物质的量浓度偏小 | |
| B. | 容量瓶用蒸馏水洗净后可以不烘干即能用于溶液的配制 | |
| C. | 所配得的NaClO消毒液在空气中光照,久置后溶液中NaClO的物质的量浓度减小 | |
| D. | 所配制NaClO溶液的物质的量浓度为2.4 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com