
现有一定量含有Na2O杂质的Na2O2试样,用下图所示的实验装置测定Na2O2试样的纯度。(可供选用的试剂只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)

回答下列问题:
(1)装置A中液体试剂选用 ,理由是 ____________________________。
(2)装置B的作用是 _________________________________________________,
装置E中碱石灰的作用是 ____________________________________________。
(3)装置D中发生反应的化学方程式是 ________,_________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为 。
科目:高中化学 来源: 题型:
下图为10 mL一定物质的量浓度的HCl溶液用一定物质的量浓度的NaOH溶液滴定的图示。请根据图示计算:
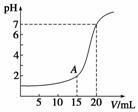
(1)氢氧化钠溶液物质的量浓度是多少?
(2)A点时溶液的pH是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
在强酸性无色透明溶液中,下列各组离子能大量共存的是( )
|
| A. | Fe3+、K+、Cl﹣、MnO4﹣ | B. | Ag+、Na+、NO3﹣、I﹣ |
|
| C. | Zn2+、Al3+、SO42﹣、Cl﹣ | D. | Ba2+、NH4+、Cl﹣、HCO3﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比KMnO4更强,本身在反应中被还原为Fe3+生成Fe(OH)3,达到净水目的,它是由Fe(NO3)3,NaOH和Cl2在一定条件下制得:
2Fe(NO3)3+16NaOH+3Cl2→□Na2FeO4+□NaNO3+□ +□H2O
(1)在横线上填上适当的物质,使制备Na2FeO4反应原理完整,并用双线桥法表示出点子转移的方向和数目 .
(2)反应使用的Fe(NO3)3可以用Fe粉和稀HNO3反应制(提示:反应过程中HNO3只被还原成NO),现在要制备Na2FeO483g的问:需要Fe粉 克,HNO3 克?
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对于过氧化钠的叙述中,正确的是( )
A.将少量Na2O2投入紫色石蕊试液中,溶液最终呈蓝色
B.1 mol Na2O2与H2O完全反应,转移2 mol电子
C.充分加热等物质的量的Na2O2和NaHCO3的混合物,剩余物质为Na2CO3
D.ag CO和H2的混合气体充分燃烧的产物与足量的Na2O2充分反应后,固体质量增加ag
查看答案和解析>>
科目:高中化学 来源: 题型:
气态PCl5的分解反应为2PCl5(g)⇌2PCl3(g)+2Cl2(g),在473K达到平衡时气态PCl5有48.5%分解,在573K达到平衡时气态PCl5有97%分解,则此反应是( )
|
| A. | 吸热反应 |
|
| B. | 放热反应 |
|
| C. | 反应的焓变为零的反应 |
|
| D. | 无法判断是吸热反应还是放热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com