
【题目】A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出),请回答下列问题:

(1)若A为短周期金厲单质,D为短周期非金厲单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为____________,反应④的化学方程式为_________________。
(2)若A是常见的变价金属的单质,D、F是气态单质,反应④可以在光照条件下发生反应①和反应②在水溶液中进行,反应②的离子方程式是__________________。
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为____________________。标准状况下3.36L物质E与含氢氧化钠10.0g的溶液充分反应,所得溶液中溶质成分为___________(写出化学式和对应的物质的量)
【答案】(1)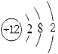 ;C+4HNO3(浓)
;C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(2)2Fe2++Cl2═2Fe3++2Cl﹣;
(3)2C+SiO2![]() Si+2CO↑;Na2CO3,0.1mol;NaHCO3,0.05mol.
Si+2CO↑;Na2CO3,0.1mol;NaHCO3,0.05mol.
【解析】
试题分析:(1)若A为短周期金属单质,D为短周期非金属单质,则A为Mg,D为C,F为硝酸,所以A的原子结构示意图为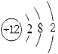 ,反应④的化学方程式为C+4HNO3(浓)==CO2↑+4NO2↑+2H2O ;(2)若A是常见的变价金属的单质,D、F是气态单质,则A为Fe,DF分别为氢气和氯气,反应②的离子方程式是2Fe2++Cl2=2Fe3++2Cl-;(3)若A、D、F都是短周期非金属元素单质,则A、D、F分别为C、Si、O,反应①的化学方程式为2C+SiO2==Si+2CO↑;标准状况下3.36LCO2的物质的量是0.15mol;10g氢氧化钠的物质的量是0.25mol,设生成碳酸钠、碳酸氢钠的物质的量分别是xmol、ymol,根据元素守恒
,反应④的化学方程式为C+4HNO3(浓)==CO2↑+4NO2↑+2H2O ;(2)若A是常见的变价金属的单质,D、F是气态单质,则A为Fe,DF分别为氢气和氯气,反应②的离子方程式是2Fe2++Cl2=2Fe3++2Cl-;(3)若A、D、F都是短周期非金属元素单质,则A、D、F分别为C、Si、O,反应①的化学方程式为2C+SiO2==Si+2CO↑;标准状况下3.36LCO2的物质的量是0.15mol;10g氢氧化钠的物质的量是0.25mol,设生成碳酸钠、碳酸氢钠的物质的量分别是xmol、ymol,根据元素守恒![]() ,得
,得![]() ,所以Na2CO3,0.1mol;NaHCO3,0.05mol。
,所以Na2CO3,0.1mol;NaHCO3,0.05mol。


科目:高中化学 来源: 题型:
【题目】微量元素在生物体内虽然含量很少,却是维持正常生命活动不可缺少的。该观点可以通过下面哪一实例得到证明?( )
A. 缺Mg时叶片变黄 B. 油菜缺少B时只开花不结果
C. 动物血液钙盐含量太低会抽搐 D. 缺P会影响ATP的吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色稀溶液X中,可能含有表所列离子中的某几种。现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂Y体积(V)的关系如图所示,下列说法正确的是
阴离子 | CO32﹣、SiO32﹣、AlO2﹣、Cl﹣ |
阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |

A.若Y是盐酸,则Oa段转化为沉淀的离子(表中,下同)只有AlO2﹣
B.若Y是盐酸,则溶液中可能含有的阳离子是Al3+
C.若Y是NaOH溶液,则bc段反应的离子方程式为
Al(OH)3+OH﹣═AlO2﹣+2H2O
D.若Y是NaOH溶液,则X溶液中只存在四种离子是:Al3+、Fe3+、NH4+、Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组欲鉴定某硫酸钠样品中是否含有亚硫酸钠,设计方案如下:取少量固体配成溶液,往溶液中滴加少量酸性KMnO4溶液,观察溶液是否褪色。

如果溶液紫色褪去,说明该样品中含有亚硫酸钠。
(1)用离子方程式表示该反应原理: 。
(2)图I表示100mL量筒中液面的位置,A与B,B与C刻度间相差10mL,如果刻度A为30,量筒中液体的体积是____________mL。图II表示25mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填字母)________________。
A.等于amL B.等于(25-a)mL C.大于amL D.大于(25-a)mL
(3)该小组同学欲测定样品中亚硫酸钠的含量,操作步骤如下:
a.称取mg样品,用蒸馏水溶解并置于锥形瓶中
b.将V1mL C1mol/L的酸性KMnO4溶液(过量)倒入锥形瓶中振荡
c.用C2mol/L草酸钠(Na2C2O4)溶液滴定过量的KMnO4,至滴定终点时用去Na2C2O4溶液V2mL
①KMnO4溶液应装在_________式滴定管中,达到滴定终点时溶液颜色的变化 。
②样品中Na2SO3的物质的量为 mol。(用含C1 、V1 、C2、 V2的代数式表示)。
(4)下列操作会导致测得的Na2SO3的物质的量偏高的是 (填字母,双选)。
A.未用Na2C2O4标准液润洗滴定管
B.滴定前仰视盛有Na2C2O4溶液的滴定管,滴定后俯视
C.滴定前滴定管尖嘴处有气泡,滴定后消失
D.滴定时摇动锥形瓶,瓶中的液滴溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+3B(g)=2C(g)+5D(g)在四种不同条件下的反应速率分别为:
① v(A)=0.8 mol·L-1·min-1 ② v(B)=0.6 mol·L-1·min-1
③ v(C)=0.3mol·L-1·min-1 ④ v(D)=1.2 mol·L-1·min-1
表示该反应速率最慢的是
A.① B.② C.③ D.④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:(1)H2(g) +1/2O2(g)=H2O(g) △H=-241.8 kJ/mol
(2)1/2N2 (g) + O2(g)=NO2(g) △H=+33.9 kJ/mol
(3)1/2N2 (g) +3/2 H2(g)=NH3(g) △H=-46.0 kJ/mol
计算NH3(g)燃烧生成NO2(g)和H2O(g)的燃烧热
A.282.8 kJ/mol B.-282.8 kJ/mol C.848.4kJ/mol D.-848.4 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是

A. 最简单气态氢化物的热稳定性:Y>X>W>Z
B. 最高价氧化物对应的水化物的酸性:X>W>Z
C. 原子半径:W>Z>Y>X
D. 元素X、Z、W的最高正价分别与其主族序数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式或离子方程式中,正确的是:
A. 甲烷的标准燃烧热为890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H="-890.3" kJ/mol
B. CO(g)的燃烧热是283.0 kJ/mol ,则2CO2(g)=2CO(g)+O2(g)的反应热△H="+2×283.0" kJ/mol
C. NaOH和HCl反应的中和热 △H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol
D. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ/mol
2NH3(g) △H=-38.6kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。
m | n | ||
x | y |
回答下列问题:
(1)元素x在周期表中的位置是 ,其单质可采用电解熔融 的方法制备。
(2)气体分子(mn)2的电子式为 ,(mn)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为 。
(3)已知氰化钠(NaCN),可以与很多金属形成络合物,因此工业上采用氰化法提炼金:用稀的氰化钠溶液处理粉碎了的金矿石,通入空气,使金矿石中的金粒溶解,生成能溶于水的络合物Na[Au(CN)2],其反应方程式为:①4Au+8NaCN+2H2O+O2=4Na[Au(CN)2]+4NaOH,Na[Au(CN)2]在水溶液中的电离方程式为:②Na[Au(CN)2]=Na++[Au(CN)2]-,然后再用锌从溶液中把金置换出来,锌转化为Na2[Zn(CN)4]。据此,请利用①写出在空气中用氰化钠溶液提取金的电极反应式:正极: ,负极: 。
(4)若人不慎氰化钠中毒,可用Na2S2O3缓解,二者反应得到两种含硫元素的离子,其中一种遇到Fe3+可变为红色。写出解毒原理的相关离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com