
| A. | 过氧化钠投入到水中:2Na2O2+2H2O=4Na++4OH-+O2↑ | |
| B. | 氯化铵溶液与浓NaOH 溶液加热:NH4++OH-=NH3•H2O | |
| C. | 氯化铝溶液中滴入过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3 NH4+ | |
| D. | 实验室制取氯气:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$ Mn2++Cl2↑+2Cl-+2H2O |
分析 A.二者反应生成氢氧化钠和氧气;
B.氯化铵溶液与浓NaOH 溶液加热生成氯化钠和氨气、水;
C.二者反应生成氢氧化铝沉淀和氯化铵;
D.氯化氢为强电解质,应拆成离子形式;
解答 解:A.过氧化钠投入到水中,离子方程式:2Na2O2+2H2O=4Na++4OH-+O2↑,故A正确;
B.氯化铵溶液与浓NaOH 溶液加热,离子方程式:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O,故B错误;
C.氯化铝溶液中滴入过量氨水,离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3 NH4+,故C正确;
D.实验室制取氯气,离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$ Mn2++Cl2↑+2H2O,故D错误;
故选:AC.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意化学式拆分,注意离子反应遵循客观事实、遵循原子个数守恒规律,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | B. | IBr+H2O═HIO+HBr | ||
| C. | 2Na2O2+4HCl═4NaCl+O2+2H2O | D. | NaH+H2O═NaOH+H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
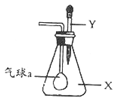 如图,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压胶头滴管的胶头,使液体滴入瓶中,振荡,套在玻璃管一端的小气球慢慢鼓起,则气体X和液体Y不可能是( )
如图,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压胶头滴管的胶头,使液体滴入瓶中,振荡,套在玻璃管一端的小气球慢慢鼓起,则气体X和液体Y不可能是( )| A. | X是氨气,Y是硫酸钠溶液 | B. | X是SO2,Y是Ba(OH)2溶液 | ||
| C. | X是CO2.Y是硫酸溶液 | D. | X是HC1,Y是氯化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KAl(SO4)2•12H2O能水解生成Al(OH)3胶体,可用作净水剂 | |
| B. | SO2有漂白、杀菌性能,可在食品加工中大量使用 | |
| C. | MnO2有较强的氧化性,可作H2O2分解的氧化剂 | |
| D. | Si是半导体材料,可用于制光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | |
| B. | 硫酸的电离方程式:H2SO4═2H++SO42- | |
| C. | S2-的结构示意图: | |
| D. | 明矾的化学式:KAl(SO4)2•12H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲醇可以使蛋白质变性,常用于食品保鲜 | |
| B. | 氧化铝熔点高,常用子制造耐火材枓 | |
| C. | 氧化钠可用作呼吸面具中的供氧剂 | |
| D. | 常温下,可用铁槽车或铝槽车运输稀硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 实验目的 | 实验操作 | |
| A | 比较水和乙醇分子中羟基上氢原子的活泼性 | 用质量相等、形状相近的金属钠分别与水和乙醇反应 |
| B | 鉴别乙烷和乙烯 | 分别将气体通入品红溶液 |
| C | 除去苯中混有的少量苯酚 | 加入足量的氢氧化钠溶液,充分振荡后分液 |
| D | 检验淀粉与稀硫酸加热后是否水解 | 加入少量新制的氢氧化铜悬浊液并加热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在水中加入少量NaHCO3固体 | B. | 在水中滴入少量稀硫酸 | ||
| C. | 在水中加入少量氯化铝固体 | D. | 将水加热到100℃,测得pH=6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com