
| A. | 柠檬在味觉上有酸味,一定含强酸性物质 | |
| B. | 氢氧化铝、氢氧化钠、碳酸钠都是常见的胃酸中和剂 | |
| C. | “地沟油”禁止食用,但处理后可用来制肥皂和生物柴油 | |
| D. | PM2.5中含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素 |
分析 A.食物的酸碱性并非指味觉上的酸碱性,也不是指化学上所指的溶液的酸碱性,而是指食物在体内代谢最终产物的性质来分类;
B.碳酸钠的腐蚀性过强,不能用于治疗胃酸过多;
C.地沟油是对生活中存在的各类劣质油的统称,长期食用可能会引发癌症,对人体的危害极大.其主要成分仍然是高级脂肪酸甘油酯,经加工处理后,可用来制肥皂和生物柴油,可以实现厨余废物合理利用;
D.砷为非金属元素.
解答 解:A.柠檬含钾、钠、钙、镁等元素,在人体内代谢后生成碱性物质,为碱性食物,故A错误;
B.氢氧化钠和碳酸钠的腐蚀性过强,对胃的刺激性过大,不能用于治疗胃酸过多,故B错误;
C.地沟油经加工处理后,可用来制肥皂和生物柴油,可以实现厨余废物合理利用,故C正确;
D.PM 2.5含有的铅、镉、铬、钒、砷等对人体有害的元素,其中铅、镉、铬、钒均是金属元素,砷为非金属元素,故D错误.
故选C.
点评 本题考查了化学知识在生活中的应用,难度不大,属于识记型知识,注意归纳总结.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,64gCu与足量浓硝酸反应恰好生成2NA个NO2分子 | |
| B. | 120gNaHSO4固体中含有NA个阳离子 | |
| C. | Si-O键的键能大于Si-Cl键的键能,因此SiO2的熔点高于晶体SiCl4的熔点 | |
| D. | CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
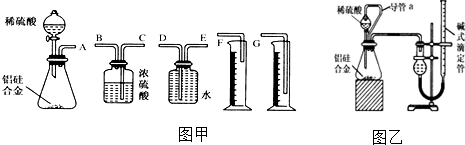
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅酸、氯化铁均为胶体 | B. | 水玻璃、氯水均为混合物 | ||
| C. | 食醋、纯碱、食盐分别属于酸、碱盐 | D. | 氨气属于非电解质,Cu属于电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
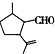 ,下列检验A中官能团的试剂和顺序正确的是( )
,下列检验A中官能团的试剂和顺序正确的是( )| A. | 先加酸性高锰酸钾溶液,后加银氨溶液,微热 | |
| B. | 先加溴水,后加酸性高锰酸钾溶液 | |
| C. | 先加银氨溶液,微热,再加入溴水 | |
| D. | 先加入新制氢氧化铜,微热.酸化后再加溴水 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
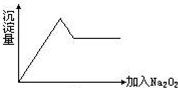 一无色透明的溶液做如下实验:
一无色透明的溶液做如下实验:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
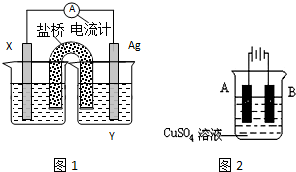
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 臭氧空洞、温室效应、光化学烟雾、硝酸型酸雨的形成都与氮氧化合物有关 | |
| B. | 石油裂解、煤的气化、海水制镁、纤维素制火棉等过程中都包含化学变化 | |
| C. | 低碳经济就是以低能耗、低污染、低排放为基础的经济发展模式 | |
| D. | 可用丁达尔效应鉴别氢氧化铁胶体和氯化铁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3和HBr | B. | Ca(HCO3)2和HNO3 | C. | Ba(NO3)2和CO2 | D. | NaHCO3和Ca(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com