
分析 (1)SiO2是非金属氧化物,而Fe2O3、Al2O3是金属氧化物,根据金属氧化物能够与酸反应的性质,用酸来除去石英沙中的Al2O3;
(2)高温下,碳和二氧化硅反应生成硅和一氧化碳;
(3)硅易被氧化成二氧化硅;反应中使用氢气,氢气若与氧气混合易引起爆炸,因此必须在无氧的氛围中进行;
故答案为:防止O2进去与H2混合引起爆炸;
(4)①提高CH4的利用率,从外界条件对平衡的影响考虑;
②依据化学平衡的三段式列式计算得到平衡浓度,结合平衡常数和转化率概念计算平衡常数K.
解答 解:(1)SiO2是非金属氧化物,而Fe2O3、Al2O3是金属氧化物能与酸反应,利用稀盐酸可以将Fe2O3、Al2O3反应除去,反应物是盐酸和Fe2O3、Al2O3,生成物是金属氯化物和水,
故答案为:HCl;
(2)高温下,碳和二氧化硅反应生成硅和一氧化碳,反应方程式为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,
故答案为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
(3)硅易被氧化成二氧化硅;反应中使用氢气,氢气若与氧气混合易引起爆炸,因此必须在无氧的氛围中进行;
故答案为:硅易被氧化成二氧化硅;防止O2进去与H2混合引起爆炸;
(4)①提高CH4的利用率,通入水蒸气、降低压强可使平衡向正反应方向移动,
故答案为:通入水蒸气、降低压强;
②在2L密闭容器中,5mol甲烷和6mol水蒸气,一段时间后,测得平衡时甲烷的转化率为40%,依据平衡三段式列式,
CH4(g)+H2O(g)?CO(g)+3H2(g)
起始量(mol) 5 6 0 0
变化量(mol) 5×40% 2 2 2×3
平衡量(mol) 5-2 6-2 2 6;
该温度下的平衡常数K=$\frac{c(CO)×{c}^{3}({H}_{2})}{c(C{H}_{4})×c({H}_{2}O)}$=$\frac{\frac{2}{2}×(\frac{6}{2})^{3}}{\frac{3}{2}×\frac{4}{2}}$=9
故答案为:9.
点评 本题考查了物质的转化和制备题,还考查了化学方程式的书写,本题考查化学平衡三段式计算应用,转化率和平衡常数的概念理解,掌握基础是解题关键,综合分析,从而得出正确的结论,要注意知识的整体性,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 两个反应中NaHSO4均为氧化产物 | |
| B. | 碘元素在反应①中被还原,在反应②中被氧化 | |
| C. | 氧化性:MnO2>SO${\;}_{4}^{2-}$>IO${\;}_{3}^{-}$>I2 | |
| D. | 反应①、②中生成等量的I2时转移电子数比为1:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤①②③④⑥⑦ | B. | ③⑤①②⑥⑦④ | C. | ③⑤②⑦①⑥④ | D. | ②⑥⑦①③⑤④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
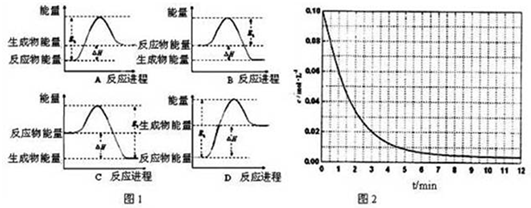
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
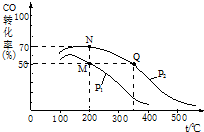 “洁净煤技术”研究在世界上相当普遍.
“洁净煤技术”研究在世界上相当普遍.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量 | |
| B. | 热化学方程式中,如果没有注明温度和压强则表示在标准状况下测得的数据 | |
| C. | 书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态 | |
| D. | 1mol碳燃烧所放出的热量为燃烧热,1mol强酸和1mol强碱完全反应所放出的热称为中和热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgCl的溶解度增大 | B. | AgCl的溶解度、溶度积KSP均不变 | ||
| C. | AgCl的溶度积KSP增大 | D. | AgCl的溶解度、溶度积KSP均增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com