
【题目】某兴趣小组为研究原电池原理,设计如图甲乙两个原电池装置。

(1)如图甲,a和b用导线连接,Cu电极的电极反应式为:________,溶液中SO42-移向______(填“Cu”或“Fe”)极。
(2)如图乙所示的原电池装置中,负极材料是_____。正极上能够观察到的现象是_______________。 负极的电极反应式是_________________。原电池工作一段时间后,若消耗负极5.4g,则放出气体______mol。
(3)将反应Cu + Fe2(SO4)3=2FeSO4 + CuSO4设计成盐桥电池并画图____________

(4)依据Ba(OH)2·8H2O与NH4Cl晶体的反应原理设计原电池,你认为是否可行并说明理由______。
【答案】2H++2e-=H2↑ Fe Al 产生气泡 Al-3e- +4OH-=AlO2- + 2H2O 0.3 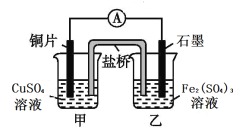 否,因为此反应为非氧化还原反应
否,因为此反应为非氧化还原反应
【解析】
(1)甲装置中,a和b用导线连接,该装置构成原电池,铁失电子发生氧化反应而作负极,铜作正极,正极上氢离子得电子发生还原反应产生氢气,电解质溶液中阴离子向负极移动,电子由铁电极经导线流向铜电极;
(2)乙装置中,铝与氢氧化钠溶液反应构成原电池,铝失电子发生氧化反应而作负极,镁作正极,正极上氢离子得电子发生还原反应产生氢气;
(3)设计原电池要满足原电池的组成条件;
(4)原电池反应必须是自发进行的放热的氧化还原反应。
(1)甲装置中,a和b用导线连接,该装置构成原电池,铁失电子发生氧化反应而作负极,铜作正极,正极上氢离子得电子发生还原反应产生氢气,电极反应式为:2H++2e-=H2↑,电解质溶液中阴离子向负极移动,溶液中SO42-移向铁电极;
(2)乙装置中,铝与氢氧化钠溶液反应构成原电池,铝失电子发生氧化反应而作负极,电极反应式为:Al-3e- +4OH-=AlO2- + 2H2O;镁作正极,正极上氢离子得电子发生还原反应产生氢气,可以观察到产生气泡;由反应总方程式可知:2Al![]() 3H2,5.4g Al的物质的量为
3H2,5.4g Al的物质的量为![]() =0.2mol,则能生成H2的物质的量为0.3mol;
=0.2mol,则能生成H2的物质的量为0.3mol;
(3)将反应Cu + Fe2(SO4)3=2FeSO4 + CuSO4设计成盐桥电池需要Cu作负极,铜电极烧杯中电解质为CuSO4,可用惰性电极作正极,电解质溶液为Fe2(SO4)3溶液,形成闭合回路,装置图为: ;
;
(4)原电池反应必须是自发进行的放热的氧化还原反应,该反应是吸热反应且不是氧化还原反应,所以不能设计成原电池。


科目:高中化学 来源: 题型:
【题目】标准状况下 ①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2 mol NH3,这四种气体的关系表达正确的是( )
a.体积②>③>①>④ b.密度②>③>④>①
c.质量②>③>①>④ d.氢原子个数①>③>④>②
A.abcB.bcdC.abdD.abcd
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞(J)是用于脑血管疾病治疗的药物。它的某种合成路线如下:
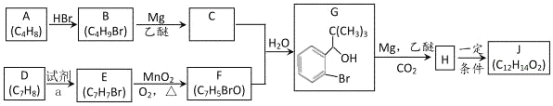
已知:
请回答下列问题:
(1)E 的名称为________,F 中所含官能团名称为_______,H→J 的反应类型为_______。
(2)B 生成 A 的方程式_______。
(3)X 是 H 的同系物,相对分子质量比 H 小 56。满足下列条件 X 的同分异构体共有_______种。
①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应。 其中核磁共振氢谱图中有五个吸收峰的同分异构体的结构简式为_______。
(4)利用题中信息所学知识,写出以甲烷和苯甲醛为原料,合成苯乙烯的路线流程图(其他无机试 剂自选)_______。合成路线流程图表达方法例如下:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,二元弱酸 H2Y 溶液中滴加 KOH 溶液,所得混合溶液的 pH 与离子浓度变化的关系如下图所示,下列有关说法错误的是

A. 曲线 M 表示 pH与 lg![]() 的变化关系
的变化关系
B. a点溶液中:c(H+) ― c(OH-)=2c(Y2-)+c(HY-) ― c(K+)
C. H2Y 的第二级电离常数Ka2(H2Y)=10-4.3
D. 交点b的溶液中:c(H2Y)=c(Y2-)>c(HY-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:

(1)第一步反应是________(填“放热”或“吸热”)反应。
(2)1mol NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中央电视台曾报道纪联华超市在售的某品牌鸡蛋为“橡皮弹”, 煮熟后蛋黄韧性胜过乒乓球,但经检测为真鸡蛋。专家介绍,这是由于鸡饲料里添加了棉籽饼,从而使鸡蛋里含有过多棉酚所致。其结构简式如图所示:下列说法不正确的是
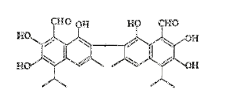
A、该化合物的分子式为:C30H30O8
B、1mol棉酚最多可与10mol H2加成,与6molNaOH反应
C、在一定条件下,可与乙酸反应生成酯类物质
D、该物质可以使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
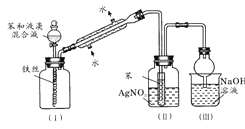
【题目】如图中A是制取溴苯的实验装置,B,C是改进后的装置,请仔细分析,对比三个装置,回答以下问题:

(1)写出三个装置中所共同发生的两个反应的化学方程式:_____;_____。写出B中盛有AgNO3溶液的试管中所发生反应的化学方程式:_____。
(2)装置A和C均采用了长玻璃导管,其作用是_____。
(3)按装置B,C装好仪器及药品后要使反应开始,应对装置B进行的操作是_____;应对装置C进行的操作是____。
(4)装置B,C较好地解决了A中加装药品和使装置及时密封的矛盾,方便了操作。A装置中这一问题在实验中造成的后果是_____。
(5)B中采用了洗气瓶吸收装置,其作用是____,反应后洗气瓶中可能出现的现象是_____。
(6)B装置也存在两个明显的缺点,使实验的效果不好或不能正常进行。这两个缺点是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学习中,有关物质性质的学习离不开实验,请阅读下列对应的内容,并按要求完成填空。
(1)实验室经常用烧杯进行性质实验研究,如图所示装置及下表中试剂,过一段时间实验1、2、3、4烧杯①中的现象分别是_____,_________,________,______。
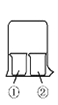
实验编号 | ①中的物质 | ②中的物质 |
1 | 淀粉碘化钾溶液 | 浓硝酸 |
2 | 酚酞溶液 | 浓硫酸 |
3 | 氯化铝溶液 | 浓氨水 |
4 | 湿润的红纸 | 饱和氯水 |
(2)用下图装置:废铜屑制硝酸铜,反应结束后,广口瓶内的溶液中,除了含有NaOH外,还有____(填写化学式)。

(3)浓氨水通常可以用于实验室快速制取氨气及其相关实验的探究,回答下列问题。

①若要测定生成的NH3的体积,则必须选择的装置是______(填装置序号),装置中所盛试剂应具有的性质是_______,收集干燥的NH3,收集装置应选择(填装置序号)_______,理由是__________。
②向浓CaCl2溶液中先通入NH3再通入CO2气体可制纳米级(粒子直径在1—10nm之间)碳酸钙,试写出制纳米级碳酸钙的离子方程式_______。
(4)下图是苯与溴发生反应并进行产物检验的反应装置:
实验装置中的冷凝管“左低右高”的放置目的是____________,整套实验装置中能防止倒吸的装置是_____(填装置序号)。
对于固体硫化钠露置在空气中的变化,有如下假设:
假设①:固体硫化钠易被空气中的氧气氧化为单质硫。
假设②:固体硫化钠易被空气中的氧气氧化为亚硫酸钠。
假设③:固体硫化钠易被空气中的氧气氧化为硫酸钠。
为了探究固体硫化钠露置在空气中究竟有怎样的变化,某化学学习小组进行了如下实验:
①从试剂瓶中取出固体硫化钠样品,放在研钵中研碎。
②将研钵中的样品露置在空气中两天。
③从研钵中取出一药匙样品放在试管中,加入盐酸,试样全部溶解,得到澄清溶液,并放出大量气泡。
④立即加塞,用力振荡,产生浑浊,且气泡的量大大减少。
(5)解释加塞振荡后产生浑浊,且气泡大量减少的原因(用化学方程式表示)________。
(6)如果要验证③是否成立的实验方法是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,改变反应物的用量或者浓度不会改变反应产物的是
A.硫粉在空气中燃烧B.澄清石灰水和碳酸氢钠溶液反应
C.锌粉加入到![]() 溶液D.氯气通入
溶液D.氯气通入![]() 溶液中
溶液中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com