
½«18 gĶŗĶĢśµÄ»ģŗĻĪļĶ¶Čė200 mLĻ”ĻõĖįÖŠ,³ä·Ö·“Ó¦ŗóµĆµ½±ź×¼×“æöĻĀ2.24 L NO,Ź£Óą9.6 g½šŹō;¼ĢŠų¼ÓČė200 mLµČÅØ¶ČµÄĻ”ĻõĖį,½šŹōĶźČ«Čܽā,ÓֵƵ½±ź×¼×“æöĻĀ2.24 L NO”£ČōĻņ·“Ó¦ŗóµÄČÜŅŗÖŠ¼ÓČėKSCNČÜŅŗ,ČÜŅŗ²»±äŗģ,ŌņĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ(””””)
| A£®Ō»ģŗĻĪļÖŠĶŗĶĢśø÷0.15 mol | B£®Ļ”ĻõĖįµÄĪļÖŹµÄĮæÅضČĪŖ1 mol”¤L-1 |
| C£®µŚŅ»“ĪŹ£Óą9.6 g½šŹōĪŖĶŗĶĢś | D£®ŌŁ¼ÓČėÉĻŹö200 mLĻ”ĻõĖį,»¹»įµĆµ½±ź×¼×“æöĻĀ2.24 L NO |
A
½āĪöŹŌĢā·ÖĪö£ŗĻņ·“Ó¦ŗóµÄČÜŅŗÖŠ¼ÓČėKSCNČÜŅŗ,ČÜŅŗ²»±äŗģ£¬ĖµĆ÷ŌŚČÜŅŗÖŠ“ęŌŚµÄĄė×ÓŹĒFe2+£»ČÜŅŗÖŠ“ęŌŚFe2+”¢Cu2+”£Į½“Ī¼ÓČėµÄĖįĻąĶ¬£¬²śÉśµÄNOµÄĪļÖŹµÄĮæĻąĶ¬£¬Ōņ×ŖŅʵĵē×ÓµÄĪļÖŹµÄĮæŅ²ĻąĶ¬”£ĆæŅ»“Ī·“Ó¦²śÉśNOµÄĪļÖŹµÄĮæĪŖ2.24L”Ā22.4L/mol=0.1mol,µē×Ó×ŖŅĘĪŖ0.1mol”Į3=0.3mol.ÓÉÓŚ½šŹō»ī¶ÆŠŌFe>Cu,ĖłŅŌŹ×ĻČČܽāµÄŹĒ½šŹōFe,øł¾Ż·“Ó¦·½³ĢŹ½ŹĒ3Fe£«8HNO3(Ļ”)=3Fe(NO3)2£«2NO”ü£«4H2O”£æÉÖŖĻūŗĵĽšŹōFedµÄĪļÖŹµÄĮæĪŖ3/2”Į0.1mol=0.15 mol.ČōŹ£ÓąµÄ½šŹō¶¼ŹĒCu£¬Ōņn(Cu)=" 9.6" g”Ā64g/mol="0.15" mol;ÓÉÓŚCuŹĒ+2¼Ū½šŹō£¬ĖłŅŌµē×Ó×ŖŅĘŹżÄæĪŖ0.15 mol”Į2=0.3mol”£ÕżŗĆÓėĢāøÉĪĒŗĻ”£Ņņ“ĖŌ»ģŗĻĪļÖŠĶŗĶĢśø÷0.15 mol”£ĆæŅ»“Ī¼ÓČėĻõĖįµÄĪļÖŹµÄĮæĪŖ8/2”Į0.1mol=0.4mol.Ņņ“ĖĻõĖįµÄĪļÖŹµÄĮæÅضČĪŖ0.4mol”Ā0.2L=2mol/L.ČōŌŁ¼ÓČėÉĻŹö200 mLĻ”ĻõĖį£¬»į·¢Éś·“Ó¦£ŗNO3-+4H++3Fe2+= 3Fe3++NO”ü+2H2O£¬n(Fe2+)=0.15 mol;·“Ó¦ŠčŅŖĻūŗÄH+µÄĪļÖŹµÄĮæĪŖ0.15 mol ”Į4/3=0.2mol;Źµ¼Ź¼ÓČėµÄn(H+)=0.4mol£¬¶ąÓŚŠčŅŖĮ棬Ņņ“Ė·Å³öµÄĘųĢå°“ÕÕFe2+Ą“¼ĘĖć”£øł¾ŻĄė×Ó·½³ĢŹ½æÉÖŖæÉ»¹»į²śÉśNOµÄµÄĪļÖŹµÄĮæĪŖ0.05 mol”£ŌŚ±ź×¼×“æöĻĀĢå»żĪŖ1.12L”£Ņņ“ĖÕżČ·Ń”ĻīĪŖA”£
æ¼µć£ŗæ¼²éĶŗĶĢśµÄ»ģŗĻĪļÓėĻõĖį·¢Éś·“Ó¦µÄĒéæöµÄÖŖŹ¶”£


 ĢģĢģĮ·æŚĖćĻµĮŠ“š°ø
ĢģĢģĮ·æŚĖćĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠÓŠ¹ŲĪļÖŹŠŌÖŹ”¢Ó¦ÓƵÄĖµ·ØÕżČ·µÄŹĒ
| A£®Š”ĖÕ“ņæÉÓėĖį·“Ó¦£¬æÉÓĆ×÷ÖĪĮĘĪøĖį¹ż¶ąµÄŅ©¼Į |
| B£®ĀČ»ÆĀĮŹĒµē½āÖŹ£¬æɵē½āĘäĖ®ČÜŅŗ»ńµĆ½šŹōĀĮ |
| C£®SO2¾ßÓŠĘư׊Ō£¬æÉÓĆÓŚ½«Ņų¶śĘÆ°×ĪŖ”°Ń©¶ś”± |
| D£®¶žŃõ»Æ¹č¾ßÓŠµ¼µēŠŌ£¬æÉÓĆÓŚÉś²ś¹āµ¼ĻĖĪ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠŅņ¹ū¹ŲĻµŠšŹöÕżČ·µÄŹĒ
| A£®SO2¾ßÓŠĘư׊Ō£¬¹ŹæÉŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ« |
| B£®ÅØĻõĖįÖŠµÄHNO3¼ū¹ā»į·Ö½ā£¬¹ŹÓŠŹ±ŌŚŹµŃéŹŅ擵½µÄÅØĻõĖį³Ź»ĘÉ« |
| C£®NaµÄ½šŹōŠŌ±ČCuĒ棬¹ŹæÉÓĆNaÓėCuSO4ČÜŅŗ·“Ó¦ÖĘČ”Cu |
| D£®FeŌŚCl2ÖŠČ¼ÉÕÉś³ÉFeCl3£¬¹ŹŌŚÓėĘäĖū·Ē½šŹō·“Ó¦µÄ²śĪļÖŠFeŅ²ĻŌ+3¼Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĮņĖįŃĒĢśŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬æÉŅŌÖʱø¶ąÖÖĪļÖŹ”£ÓŠ¹ŲĻĀĮŠÖʱø·½·Ø“ķĪóµÄŹĒ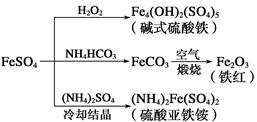
| A£®Öʱø¼īŹ½ĮņĖįĢśĄūÓĆĮĖ¹żŃõ»ÆĒāµÄŃõ»ÆŠŌ |
| B£®ĪŖ·ĄÖ¹NH4HCO3·Ö½ā£¬Éś²śFeCO3ŠčŌŚ½ĻµĶĪĀ¶ČĻĀ½ųŠŠ |
| C£®æÉÓĆKSCNČÜŅŗ¼ģŃé(NH4)2Fe(SO4)2ŹĒ·ń±»Ńõ»Æ |
| D£®Öʱø(NH4)2Fe(SO4)2ĄūÓĆĮĖĖüµÄČܽā¶Č±ČFeSO4µÄČܽā¶Č“óÕāŅ»ŠŌÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
½«Ņ»¶ØĮæµÄĀČĘųĶØČė30mLÅضČĪŖ10.00 mol”¤L-1µÄNaOHÅØČÜŅŗÖŠ£¬¼ÓČČÉŁŠķŹ±¼äŗóČÜŅŗÖŠŠĪ³ÉNaCl”¢NaClO”¢NaClO3¹²“ęĢåĻµ”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
| A£®ÓėNaOH·“Ó¦µÄĀČĘųŅ»¶ØĪŖ0.3mol |
| B£®n(Na+):n(Cl-)æÉÄÜĪŖ7£ŗ3 |
| C£®Čō·“Ó¦ÖŠ×ŖŅʵĵē×ÓĪŖn mol £¬Ōņ0.15£¼n£¼0.25 |
| D£®n(NaCl):n(NaClO):n(NaClO3)æÉÄÜĪŖ11£ŗ2£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
NaClŹĒŅ»Öֻƹ¤ŌĮĻ£¬æÉŅŌÖʱøŅ»ĻµĮŠĪļÖŹ(ČēĶ¼ĖłŹ¾)”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ 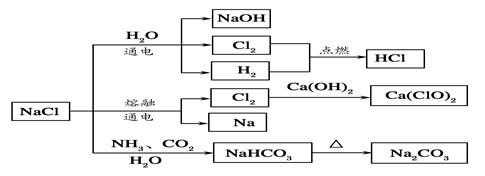
| A£®25”ę£¬NaHCO3ŌŚĖ®ÖŠµÄČܽā¶Č±ČNa2CO3µÄ“ó |
| B£®ŹÆ»ŅČéŗĶCl2·“Ó¦æÉÖʵĆĘÆ°×·Ū£¬ĘäÖ÷ŅŖ³É·ÖŹĒ“ĪĀČĖįøĘ |
| C£®³£ĪĀĻĀøÉŌļµÄCl2ÄÜÓĆøÖĘæÖü“ę£¬ĖłŅŌCl2²»ÓėĢś·“Ó¦ |
| D£®ČēĶ¼ĖłŹ¾×Ŗ»Æ·“Ó¦²»¶¼ŹĒŃõ»Æ»¹Ō·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ČēĶ¼ŹĒ¹¤ŅµÖĘ“æ¼īµÄ²æ·ÖĪļÖŹ×Ŗ»ÆŹ¾ŅāĶ¼£¬ĻĀĮŠĶĘ²ā“ķĪóµÄŹĒ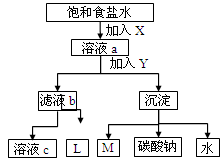
| A£®ČōŹĒĮŖ¼ī·Ø£¬ČÜŅŗcæÉŌŚ×Ŗ»ÆĮ÷³ĢÖŠŃ»·ĄūÓĆ |
| B£®ČōŹĒ°±¼ī·Ø£¬ŌņLµÄÖ÷ŅŖ³É·ÖŹĒNaCl |
| C£®MæÉŌŚ×Ŗ»ÆĮ÷³ĢÖŠŃ»·ĄūÓĆ |
| D£®XŹĒNH3£¬YŹĒCO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
¢ŁĻņ50mLl8mol”¤L-1µÄH2SO4ČÜŅŗÖŠ¼ÓČĖ×ćĮæµÄĶʬ¼ÓČČ³ä·Ö·“Ó¦ŗ󣬱»»¹ŌµÄH2SO4µÄĪļÖŹµÄĮæµČÓŚ0.45mol
¢Ś±ź×¼×“æöĻĀ£¬0.5NAøöNOŗĶ0.5NAøöO2»ģŗĻĘųĢåµÄĢå»żŌ¼ĪŖ22.4 L
¢ŪĻņČÜŅŗÖŠµĪČėĀČ»Æ±µČÜŅŗ£¬ŌŁ¼ÓĻ”ĻõĖįÄܼģŃéČÜŅŗÖŠŹĒ·ńŗ¬ÓŠSO42-
¢ÜÓƶ”“ļ¶ūĻÖĻóæÉŅŌĒų·ÖŹ³ŃĪĖ®ŗĶµķ·ŪČÜŅŗ
¢ŻŌŚŹ¹AlČܽā²śÉśH2µÄČÜŅŗÖŠÄÜ“óĮæ“ęŌŚ£ŗNH4+”¢Na+”¢Fe2+”¢NO3-
| A£®¢Ł¢Ś¢Ū¢Ż |
| B£®¢Ł¢Ū¢Ü |
| C£®¢Ü |
| D£®¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠĪļÖŹµÄ×Ŗ»ÆŌŚøų¶ØĢõ¼žĻĀÄÜŹµĻֵďĒ
¢Ł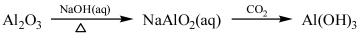
¢Ś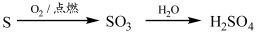
¢Ū
¢Ü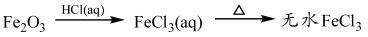
¢Ż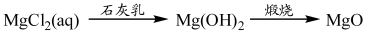
| A£®¢Ł¢Ū¢Ż | B£®¢Ś¢Ū¢Ü | C£®¢Ś¢Ü¢Ż | D£®¢Ł¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com