
硒是一种非金属,可以用作光敏材料、电解锰行业催化剂。
(l)Se是元素周期表中第34号元素,其基态原子的核外电子排布式为 。
(2)根据价层电子对互斥理论,可以推知SeO3的分子空间构型为 ,其中Se原子采用的轨道杂化形式为 。
(3)CSe2与CO2结构相似,CSe2分子内σ键与π键个数之比为 。CSe2首次是由H2Se与CCl4反应后制取的,CSe2分子内的Se—C—Se键角 (填“大于”,“等于”或“小于”)H2Se分子内的H—Se—H键角。
(4)硒化铷晶体属于反萤石型结构,晶胞结构如图所示。每个晶胞中包含 个Rb2Se单元,其中Se2-周围与它距离最近且相等的Rb+的离子数目为 。
(8分)(1)1s22s22p63s23p63d104s24p4(2分)
(2)平面三角形;sp2(2分)
(3)1:1;大于(2分)
(4)4;8(2分)
解析试题分析:(l)硒是34号元素,基态原子核外有34个电子,所以根据构造原理可知,其基态原子核外电子排布式为1s22s22p63s23p63d104s24p4。
(2)根据价层电子对互斥理论可知,SeO3的分子中中心原子含有的孤对电子对数=(6-3×2)÷2=0。这说明分子中含有3个价层电子对,且没有孤电子对,所以其空间构型是平面三角形,采用sp2杂化。
(3)二氧化碳分子中含有2个碳氧双键,单键都是σ键,双键是由1个σ键与1个π键构成的,所以CO2分子内σ键与π键个数之比为2:2=1:1。CSe2与CO2结构相似,所以CSe2分子内σ键与π键个数之比也是1:1。二氧化碳是直线型分子,H2Se分子与水分子的空间构型相似,剩余v型分子,所以CSe2分子内的Se-C-Se键角大于H2Se分子内的H-Se-H键角。
(4)根据晶胞的结构可知,白色球都在晶胞内部,所以该晶胞中含有白色球个数=8,黑色球个数=8× +6×
+6×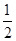 =4,所以每个晶胞中包含4个Rb2Se单元。由于1个面被8个面共用,根据晶胞结构可知,最上面面心上的Se2-距离最近且相等的Rb+的离子数目是8个。
=4,所以每个晶胞中包含4个Rb2Se单元。由于1个面被8个面共用,根据晶胞结构可知,最上面面心上的Se2-距离最近且相等的Rb+的离子数目是8个。
考点:考查核外电子排布、空间构型、杂化轨道以及晶体化学式确定等


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
某化学式为AB的离子晶体,已知5r(A2+)=4r(B2-)(各类离子晶体与 关系如下图所示),经测定其密度为
关系如下图所示),经测定其密度为 g·cm-3,其摩尔质量为Mg·mol-1,则下列有关该晶体的说法正确的是( )
g·cm-3,其摩尔质量为Mg·mol-1,则下列有关该晶体的说法正确的是( )
| r+/r- | 配位数 | 实例 |
| 0.225~0.414 | 4 | ZnS |
| 0.414~0.732 | 6 | NaCl |
| 0.732~1.0 | 8 | CsCl |
| >1.0 | 12 | CsF |
 cm
cm查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(6)某离子晶体的晶胞结构如图所示。试求:
(1)晶体中每一个X同时吸引着________Y,每个Y同时吸引着________个X,该晶体的化学式是________________________。
(2)晶体中在每个X周围与它最接近且距离相等的X共有________个。
(3)晶体中距离最近的2个X与一个Y形成的夹角(∠XYX)为________。
(4)设该晶体的摩尔质量为M g·mol-1,晶体密度为ρ g·cm-3,阿伏加德罗常数为NA,则晶体中两个距离最近的X的核间距离为________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
Ⅰ.已知下列金属晶体:Na、Po、K、Fe、Cu、Mg、Zn、Au。其堆积方式为:
(1)简单立方堆积的是____________________________________________;
(2)钾型的是______________________________________________________;
(3)镁型的是______________________________________________________;
(4)铜型的是_____________________________________________________。
Ⅱ.A、B、C、D都是短周期元素,原子半径D>C>A>B,已知:A、B处于同一周期,A、C处于同一主族;C原子核内的质子数等于A、B原子核内的质子数之和;C原子最外层电子数是D原子最外层电子数的4倍。
试回答:
(1)这四种元素分别是:A______,B______,C______,D______(填元素名称)。
(2)这四种元素单质的熔点由高到低的顺序是________(填元素名称)。
(3)C的固态氧化物是________晶体,D的固态单质是________晶体。
(4)写出A、B、D组成的化合物与B、C组成的化合物相互反应的化学方程式_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
从原子、分子水平上帮助我们认识物质构成的规律;以微粒之间不同的作用力为线索,研究不同类型物质的有关性质;从物质结构决定性质的视角预测物质的有关性质。
(1)下列说法正确的是 (填序号)。
| A.元素电负性由大到小的顺序为:F>O>N |
| B.一个苯分子含3个π键和6个σ键 |
| C.氯化钠和氯化铯晶体中氯离子的配位数相同 |
| D.第一电离能的大小为:Br>Se>As |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知反应A+B=C+D的能量变化如右图所示,下列说法正确的是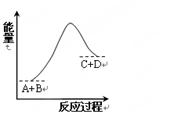
| A.该反应为放热反应 |
| B.该反应为吸热反应 |
| C.反应物的总能量高于生成物的总能量 |
| D.该反应只有在加热条件下才能进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氢气在氯气中燃烧时产生苍白火焰。在反应过程中,破坏1mol氢气中的化学键消耗的能量为 kJ,破坏1mol氯气中的化学键消耗的能量为
kJ,破坏1mol氯气中的化学键消耗的能量为 kJ,形成1mol氯化氢中的化学键释放的能量为
kJ,形成1mol氯化氢中的化学键释放的能量为 kJ。下列关系式中正确的是( )
kJ。下列关系式中正确的是( )
A. | B. | C. | D. |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列属于吸热反应的是
| A.CaO + H2O = Ca(OH)2 | B.C + H2O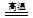 CO + H2 CO + H2 |
| C.NaOH + HCl =" NaCl" + H2O | D.2Mg + CO2 2MgO + C 2MgO + C |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.7.8克Na2S和Na2O2的固体混合物中含有的阴离子数目为0.1NA |
B.用铜做电极电解CuSO4溶液的反应方程式: 2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
| C.常温时,浓度均为0.01mol/L的 Na2CO3溶液和NaHCO3溶液等体积混合,其溶液中粒子浓度关系为c(CO32-) +c(HCO3-)+c(H2CO3) =0.02mol/L |
| D.在蒸馏水中滴加浓H2SO4,KW不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com