
����Ŀ�����Ĺ̶��Լ����ð��ϳ����������������Ǽ���������ѧ��һֱ�о��Ŀ��⡣
(1)�±��о��˲�ͬ�¶��´����̵���ҵ�̵��IJ���Kֵ��
��Ӧ | �����̵� N2(g)��O2(g) | ��ҵ�̵� N2(g)��3H2(g) | |||
�¶�/�� | 27 | 2 000 | 25 | 400 | 450 |
K | 3.8��10��31 | 0.1 | 5��108 | 0.507 | 0.152 |
�ٷ������ݿ�֪�������̵���Ӧ����____________(����ȡ����ȡ�)��Ӧ��
�ڷ������ݿ�֪������ʺϴ��ģģ������̵���ԭ��______________________________________��
����500 �桢2.02��107 Pa��������������һ�ܱ������г���1 mol N2��3 mol H2����ַ�Ӧ�ų�������________(����ڡ�����С�ڡ����ڡ�)92.4 kJ��
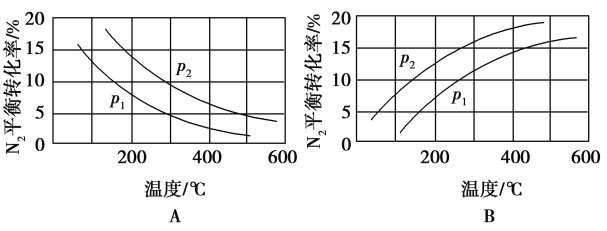
(2)��ҵ�̵���Ӧ�У�������������ͬʱ���ֱ�ⶨN2��ƽ��ת�����ڲ�ͬѹǿ(p1��p2)�����¶ȱ仯�����ߣ���ͼ��ʾ��ͼʾ�У���ȷ����___________(�A����B��)���Ƚ�p1��p2�Ĵ�С��ϵ��___________��
(3)��һ���¶��£���1 mol N2��3 mol H2����������������ܱ������з�����ҵ�ϳɰ���Ӧ���ﵽƽ��״̬ʱ��������������ʵ���Ϊ2.8 mol��
�ٴ�ƽ��ʱ��H2��ת���ʦ�1��_____________��
����֪ƽ��ʱ������ѹǿΪ8MPa����ƽ�ⳣ��Kp��_________________��(��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ����ѹ�����ʵ�������)��
��Ϊ���H2��ת���ʣ�ʵ���������˲�ȡ�Ĵ�ʩ��______________(����ĸ)��
A�������¶� B�����ʺϴ������Ե��ʵ����� C���ʵ�����ѹǿ
D����Сѹǿ E��ѭ�����úͲ��ϲ��䵪�� F����ʱ�Ƴ���
���𰸡����� KֵС��������еij̶�С(��ת���ʵ�)�����ʺϴ��ģ���� С�� A p2>p1 60% 49/192(MPa)2 CEF
��������
��1�����¶�Խ�ߣ�KԽ��˵�������¶ȣ�ƽ�����ƣ�
��Kֵ��С��ת���ʺ�С��
���Ȼ�ѧ��Ӧ��ָ��ȫת������ЧӦ�������淴Ӧ������ȫת����
��2���ϳɰ���ӦΪ���ȷ�Ӧ�������¶ȣ�ת���ʼ�С������ѹǿƽ�������ƶ���ת��������
��3��������ƽ������ʽ����ʽ������
������ƽ��ʱ�����ʵ�ѹǿ֮�ȵ��������ʵ���֮�ȼ��㣻
�����ݻ�ѧƽ���ƶ�ԭ��������
��1�����ɱ������ݿ�֪���¶�Խ�ߣ�KԽ��˵�������¶ȣ�ƽ�����ƣ�������Ӧ����Ϊ���ȷ�Ӧ���ʴ�Ϊ�����ȣ�
���ɱ������ݿ�֪�����¶����ߵ�2000��ʱ��K=0.1��Kֵ��С����ת���ʺ�С�����ʺϴ��ģ��������������ʺϴ��ģģ������̵����ʴ�Ϊ��KֵС��������еij̶�С����ת���ʵͣ������ʺϴ��ģ������
���Ȼ�ѧ��Ӧ��ָ��ȫת������ЧӦ�������淴Ӧ������ȫת��������һ�ܱ������г���1molN2��3molH2����ַ�Ӧ�ų�������С��92.4kJ��
��2���ϳɰ���ӦΪ���ȷ�Ӧ�������¶ȣ�ת���ʼ�С������ͼA��ȷ��B���÷�Ӧ������Ϊ�����С�ķ�������ѹǿƽ�������ƶ���ת����������2��ת���ʴ�����2�ʴ�Ϊ��A����2����1��
��3������μӷ�Ӧ�ĵ������ʵ���Ϊxmol��
�÷�Ӧ��N2��g��+3H2��g��![]() 2NH3��g��
2NH3��g��
��ʼ��mol��1 3 0
�仯��mol�� x 3x 2x
ƽ�⣨mol�� 1-x 3-3x 2x
��ʽ�ɵã���1-x��+��3-3x��+2x=2.8��x=0.6��
����ת����=![]() ��100%=60%�������뷴Ӧ������ʵ���֮�ȵ����������֮��ʱ����Ӧ���ת�������������������ת����Ҳ��60%��
��100%=60%�������뷴Ӧ������ʵ���֮�ȵ����������֮��ʱ����Ӧ���ת�������������������ת����Ҳ��60%��
��ƽ��ʱ�����ʵ�ѹǿ֮�ȵ��������ʵ���֮�ȣ�����P��N2��=![]() ��8MPa=
��8MPa=![]() MPa��
MPa��
P��H2��=![]() ��8MPa=
��8MPa=![]() MPa��
MPa��
P��NH3��=![]() ��8MPa=
��8MPa=![]() MPa��
MPa��
��ѧƽ�ⳣ��Kp=![]() =
=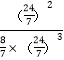 =
=![]() (MPa)2=0.26(MPa)2��
(MPa)2=0.26(MPa)2��
��������Ӧ���Ũ�ȣ������������Ũ�ȣ�����ѹǿ�������¶ȹ�ҵ�ϳɰ���Ӧ������Ӧ�����ƶ���������ת������ߣ�����ʵ�������в����õ��£���Ϊ�¶ȵͻ�ѧ��Ӧ���������ʴ�Ϊ��CEF��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�Ϊ2 L���ܱ������У��з�ӦmA(g)��nB(g) ![]() pC(g)��qD(g)������5 min�ﵽƽ�⣬��ʱ�����ʵı仯ΪA���ʵ���Ũ�ȼ���a mol��L��1��B��ƽ����Ӧ����v(B)��a/15 mol��L��1��min��1��C���ʵ���Ũ������2a/3 mol��L��1����ʱ������ϵͳѹǿ������A��C�İٷֺ������䣬��m��n��p��qΪ(����)
pC(g)��qD(g)������5 min�ﵽƽ�⣬��ʱ�����ʵı仯ΪA���ʵ���Ũ�ȼ���a mol��L��1��B��ƽ����Ӧ����v(B)��a/15 mol��L��1��min��1��C���ʵ���Ũ������2a/3 mol��L��1����ʱ������ϵͳѹǿ������A��C�İٷֺ������䣬��m��n��p��qΪ(����)
A. 3��1��2��2B. 1��3��2��2C. 1��3��2��1D. 1��1��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������̼����ȼ�ϵ��ԭ��ʾ����ͼ�������йظõ�ص�˵����ȷ����
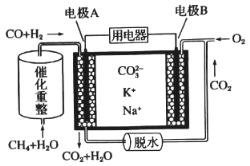
A. ��ع���ʱ,CO32-��缫B�ƶ�
B. �缫A��H2����ĵ缫��ӦΪH2+2OH--2e-=2H2O
C. ��ӦCH4+H2O![]() 3H2+CO,ÿ����1 mol CH4�μӷ�Ӧ��ת��6mol����
3H2+CO,ÿ����1 mol CH4�μӷ�Ӧ��ת��6mol����
D. �缫B�Ϸ����ĵ缫��ӦΪO2+4e-+2H2O=4OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£��ݻ�һ�����ܱ������з�����ӦA(s)+2B(g)![]() C(g)+D(g)�����������������ٷ����仯ʱ��������Ӧ�Ѵ�ƽ�����
C(g)+D(g)�����������������ٷ����仯ʱ��������Ӧ�Ѵ�ƽ�����
�����������ܶ� ����������ѹǿ ��B�����ʵ���Ũ�� ���������������ʵ���
A. �٢� B. �ڢ� C. �٢� D. �٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������A������ͼ��������Է�������Ϊ84��������ױ��������к���̼̼˫�����˴Ź����ױ���������ֻ��һ�����͵��⡣�Ľṹ��ʽΪ
A. CH3CH=CHCH3
B. 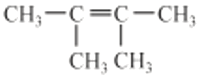
C. CH3CH2CH=CHCH3
D. CH2=CHCH2CH2CH2CH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����������ȼ�ϵ�ؿ�������ˮ��������ˮ�������乤��ԭ����ͼ��ʾ������˵������ȷ����
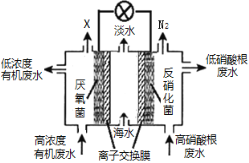
A. �м���Cl���������� B. ������ĺ��������ˮpH����
C. X����ΪCO2 D. ��·��ÿͨ��1 mol���ӣ�������״���µ��������Ϊ2.24L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ƿ��ֽ��Ǵ�������һ�ֳ�֮Ϊ�ʻ���(COS)�ķ��ӣ���ṹ��CO2���ƣ��ʻ�����һ��������������ص����ʣ������Ʋⲻ��ȷ����( )
A. COS�Ǻ��м��Լ��Ĺ��ۻ�����B. COS�ķе��CO2��
C. COS ����ʽΪ![]() D. COS������ԭ������8�����ȶ��ṹ
D. COS������ԭ������8�����ȶ��ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���к��Ȳⶨʵ���У����в�����ʹ��õ�HƫС���ǣ� ��
A.���ձ���û�и�Ӳֽ��
B.�û���ͭ˿��������滷�β��������
C.����ͬŨ�Ⱥ�������������ϡ������Һ����ʵ��
D.��1gNaOH�������50mL0.5mol/L��NaOH��Һ����ʵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ3A(g)+B(g)![]() 2C(g)+2D(s)��2 L�ܱ������н��У�����4min��B������0.4 mol����0��4min�ڴ˷�Ӧ��ƽ������Ϊ
2C(g)+2D(s)��2 L�ܱ������н��У�����4min��B������0.4 mol����0��4min�ڴ˷�Ӧ��ƽ������Ϊ
A. v(A)=0.15 mol��L1B. v(B)=0.05 mol��L1��s1
C. v(C)=0.10 mol��L1��min1D. v(D)=0.10 mol��L1��min1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com