
可溶性钡盐有毒,医院中常用硫酸钡这种钡盐作为内服造影剂。医院抢救钡离子中毒患者时,除催吐外,还需要向中毒者胃中灌入硫酸钠溶液。
已知:Ksp(BaCO3)=5.1×10-9;Ksp(BaSO4)=1.1×10-10
下列推断中正确的是( )
A.不用碳酸钡作为内服造影剂,是因为Ksp(BaCO3)>Ksp(BaSO4)
B.抢救钡离子中毒患者时,若没有硫酸钠,可以用碳酸钠溶液代替
C.若误饮c(Ba2+)=1.0×10-5mol·L-1的溶液时,会引起钡离子中毒
D.可以用0.36 mol·L-1的Na2SO4溶液给钡离子中毒患者洗胃
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案科目:高中化学 来源: 题型:
如图所示的两个实验装置中,溶液的体积均为200 mL,开始时电解质溶液的浓度均为0.1 mol·L-1,工作一段时间后,测得两端导线中均通过0.02 mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )

A.产生气体的体积:①>②
B.两极上析出物质的质量:②>①
C.溶液的pH变化:①增大,②减小
D.电极反应式①中阳极:4OH-—→2H2O+O2↑+4e-;②中阴极:2H++2e-—→H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
关于聚四氟乙烯的下列说法中,错误的是 ( )。
A.能够耐强酸、强碱甚至“王水”的腐蚀
B.摩擦系数小,极其光滑,可以减少与雪或水的摩擦力
C.由单体发生缩聚反应而制得的
D.耐高温又耐低温,绝缘性好,在水中也不会被浸湿或膨胀
查看答案和解析>>
科目:高中化学 来源: 题型:
有效地利用现有能源和开发新能源已受到各国的普 遍重视。改进汽油组成的办法可用来改善汽油的燃烧性能。例如,加入CH3OC(CH3)3来生产“无铅汽油”。CH3OC(CH3)3分子中必存在的原子间连接形式有 ( )。
遍重视。改进汽油组成的办法可用来改善汽油的燃烧性能。例如,加入CH3OC(CH3)3来生产“无铅汽油”。CH3OC(CH3)3分子中必存在的原子间连接形式有 ( )。
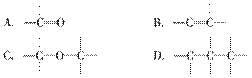
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=12.0,则下列说法不正确的是( )
A.所得溶液中的c(H+)=1.0×10-12 mol·L-1
B.所加的烧碱溶液pH=12.0
C.所得溶液中由水电离产生的c(OH-)=1.0×10-12 mol·L-1
D.所得溶液中的c(Mg2+)=5.6×10-8 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol·L-1)如图所示:
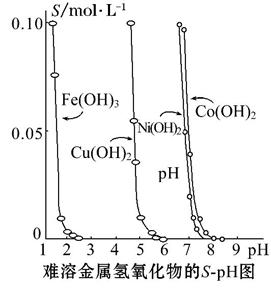
(1)pH=3时溶液中铜元素的主要存在形式是 。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH 。
A.<1 B.4左右 C.>6
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质, ______(填“能”或“不能”)通过调节溶液pH的方法来除去,理由是 。
(4)已知一些难溶物的溶度积常数如下表:
| 物质 | FeS | MnS | CuS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-35 |
| Ksp | 3.4×10-28 | 6.4×10-33 | 1.6×10-24 |
为除去某工业废水中含有的Cu2+、Pb2+、Hg2+杂质,最适宜向此工业废水中加入过量的 。
A.NaOH B.FeS C.Na2S
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于常温下,pH=3的醋酸溶液(I)和 pH=11的氢氧化钠溶液(Ⅱ)的说法正确的是( )
A.I和Ⅱ的物质的量浓度均为0.001mol·L-1
B.将I稀释10倍,溶液中 c(CH3COOH)、 c(OHˉ)均减小
C.I和Ⅱ溶液混合,若c(OH-)>c(H+),则氢氧化钠过量
D.I和Ⅱ等体积混合后,溶液中离子浓度大小为c(CH3COO-)c(Na+)> c(H+)> c(OH--)
查看答案和解析>>
科目:高中化学 来源: 题型:
三氧化二镍(Ni2O3)是一种重要的电子元件材料和蓄电池材料。工业上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍(NiC2O4·2H2O),再高温煅烧草酸镍制取三氧化二镍。已知草酸的钙、镁、镍盐均难溶于水。根据下列工艺流程示意图回答问题。
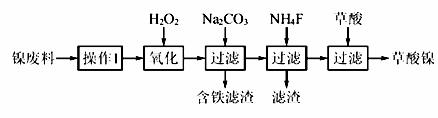
(1)操作1为 。
(2)生产过程中多次进行过滤,实验室进行过滤操作中需用到玻璃棒,下列实验操作中哪些操作中玻璃棒的作用完全相同的是 (填选项字母)。
①配制0.1mol/L的H2SO4溶液
②测定Na2CO3溶液的pH
③用KI淀粉试纸检验溶液中的氧化性离子
④加热食盐溶液制备NaCl晶体
⑤配制20%的KNO3溶液
A.①⑤ B.②③ C.④⑤ D.①④
(3)加入H2O2发生的主要反应的离子方程式为 ;加入Na2CO3溶液调pH至4.0~4.5,其目的为 ; 加入NH4F后除掉的杂质是 。
加入NH4F后除掉的杂质是 。
(4)草酸镍(NiC2O4·2H2O)在热空气中干燥脱水后在高温下煅烧三小时,制得Ni2O3,同时获得混合气体。草酸镍受热分解的化学方程式为 。
(5)工业上还可用电解法制取Ni2O3。用NaOH溶液调节NiCl2溶液的pH至7.5,加入适量Na2SO4后采用惰性电极电解。电解过程中产生的Cl2有80%在弱碱性条件下生成ClO-,再把二价镍氧化为三价镍。ClO-氧化Ni(OH)2生成Ni2O3的离子方程式为 。amol二价镍全部转化为三价镍时,外电路中通过电子的物质的量为 。
(6)电解法制取Ni2O3的实际过程中,有时获得一种结晶水合物,已知含1molNi的该物质中含有0.5mol结晶水。取该化合物20.2g进行充分加热,获得Ni2O3固体和0.2mol水,则该结晶水合物的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
今有A、B两种元素的原子,已知A原子M层有x个电子,N层有y个电子,B原子的M层有(x+5)个电子,N层有(y+5)个电子,则A、B分别是 (填写元素符号)_____________,其电子排布式分别为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com