
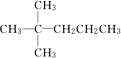
 ,该烷烃分子的名称2,2-二甲基戊烷C7H16另一种同分异构体分子是由烯烃和氢气加成得到,而且该烯烃分子中的碳碳双键只有一种位置,试写出这种烯烃分子的名称3,3-二甲基-1-戊烯.
,该烷烃分子的名称2,2-二甲基戊烷C7H16另一种同分异构体分子是由烯烃和氢气加成得到,而且该烯烃分子中的碳碳双键只有一种位置,试写出这种烯烃分子的名称3,3-二甲基-1-戊烯. 分析 该有机物为烷烃,可以通过让两个甲基按照由心到边移动,即可得到同分异构体的结构简式;其中有一种同分异构体的分子,其一氯代物有4种同分异构体,也就是分子结构中有四种氢,写出其结构简式利用烷烃的系统命名法命名;某种烃与H21:1加成得到烷烃,则该烃分子中含有1个碳碳双键,根据加成原理采取逆推法还原C=C双键,烷烃分子中相邻碳原子上均带氢原子的碳原子间是对应烯烃存在碳碳双键的位置.
解答 解:根据已知有机物的结构简式可判断,可以通过让两个甲基按照由心到边移动,即可得到同分异构体的结构简式,所以共计是4种、分别是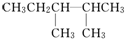 、
、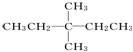 、
、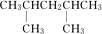 、
、 ,其中有四种不同的氢的是名称分别是2,3二甲基戊烷,另一种同分异构体分子是由烯烃和氢气加成得到,而且该烯烃分子中的碳碳双键只有一种位置,说明相邻碳上有氢,而且对称,则是3,3二甲基戊烷对应的烯烃为:3,3-二甲基-1-戊烯,
,其中有四种不同的氢的是名称分别是2,3二甲基戊烷,另一种同分异构体分子是由烯烃和氢气加成得到,而且该烯烃分子中的碳碳双键只有一种位置,说明相邻碳上有氢,而且对称,则是3,3二甲基戊烷对应的烯烃为:3,3-二甲基-1-戊烯,
故答案为:4; ;2,2-二甲基戊烷; 3,3-二甲基-1-戊烯.
;2,2-二甲基戊烷; 3,3-二甲基-1-戊烯.
点评 本题考查有机物结构与性质、结构简式、有机物的命名等,为高考种的常见考点之一,题目难度中等,试题基础性强,贴近高考,注重解题方法的指导与训练,有助于培养学生的逻辑推理能力和逆向思维能力,注意掌握常见有机物结构与性质.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
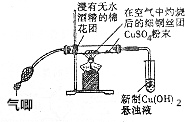 在完成“乙醇的催化氧化实验“后,某学校化学兴趣小组认为该实验方案存在着明显的缺点.
在完成“乙醇的催化氧化实验“后,某学校化学兴趣小组认为该实验方案存在着明显的缺点.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a+8+m-n | B. | a+18-m+n | C. | a+32-m-n | D. | a+24-m-n |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
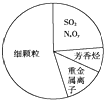
| A. | SO2和NxOy都属于酸性氧化物 | |
| B. | 雾属于胶体,能产生丁达尔效应 | |
| C. | 重金属离子可导致蛋白质变性 | |
| D. | 汽车尾气的大量排放是造成雾霾天气的人为因素之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Al | Si | S | Cl | Ar |
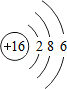 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
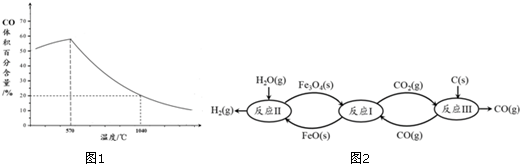

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
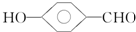 的沸点比
的沸点比 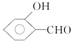 高,原因是
高,原因是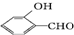 形成分子内氢键,而
形成分子内氢键,而 形成分子间氢键,分子间氢键使分子间作用力增大.
形成分子间氢键,分子间氢键使分子间作用力增大.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com