
| N |
| NA |
| m |
| M |
| 6.02×1023 |
| 6.02×1023mol-1 |
| 44g |
| 2g/mol |


 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案科目:高中化学 来源: 题型:
| A、25℃101kPa时,CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-Q kJ/mol,则甲烷的燃烧热为Q kJ/mol |
| B、CaCO3(s)=CaO(s)+CO2(g) 室温下不能自发进行,说明该反应的△H<0 |
| C、反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡后,升高温度,反应速率v(H2)和H2的平衡转化率均增大 |
| D、已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2的值均大于零): H2(g)+Cl2(g)=2HCl(g)△H1=-Q1 kJ/mol H2(g)+Br2(g)=2HBr(g)△H2=-Q2 kJ/mol 则△H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
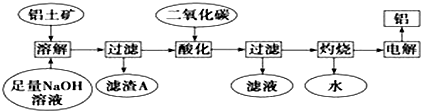
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是某学校实验室从化学试剂商店买回来的氢氧化钠试剂标签上的部分内容.某同学从该试剂瓶中取出24.0g固体,配成500mL溶液,请计算
如图是某学校实验室从化学试剂商店买回来的氢氧化钠试剂标签上的部分内容.某同学从该试剂瓶中取出24.0g固体,配成500mL溶液,请计算查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到 |
| D、日常生活中无水乙醇常用于杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
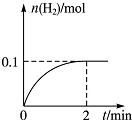 化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理.请回答下列问题:
化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com