
【题目】微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示,下列说法正确的是

A. HS-在硫氧化菌作用下转化为SO42-的反应为:HS-+4H2O-8e-== SO42-+9H+
B. 电子从b流出,经外电路流向a
C. 如果将反应物直接燃烧,能量的利用率不会变化
D. 若该电池电路中有0.4mol电子发生转移,则有0.5molH+通过质子交换膜
【答案】A
【解析】由图可知硫酸盐还原菌可以将有机物氧化成二氧化碳,而硫氧化菌可以将硫氢根离子氧化成硫酸根离子,所以两种细菌存在,就会循环把有机物氧化成CO2 放出电子,负极上HS-在硫氧化菌作用下转化为SO42-,失电子发生氧化反应,电极反应式是HS-+4H2O-8e-=SO42-+9H+;正极上是氧气得电子的还原反应:4H++O2+4e-=2H2O。A、负极上HS-在硫氧化菌作用下转化为SO42-,失电子发生氧化反应,电极反应式是HS-+4H2O-8e-=SO42-+9H+,选项A正确;
B、b是电池的正极,a是负极,电子从a流出,经外电路流向b,选项B错误;C、如果将反应物直接燃烧,部分能量转化为光能或热能等,能量的利用率发生变化,选项C错误;D、根据电子守恒,若该电池有0.4mol电子转移,有0.4molH+通过质子交换膜,选项D错误。答案选A。


科目:高中化学 来源: 题型:
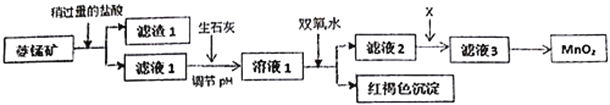
【题目】工业上用菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等杂质]为原料制取二氧化锰,其流程示意图如下:
已知:生成氢氧化物沉淀的pH
Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
Ksp(CuS)=6.3×10-16 Ksp(MnS)= 3×10-14
注:金属离子的起始浓度为0.1 mol/L
回答下列问题:
(1)含杂质的菱锰矿使用前需将其粉碎,主要目的是_________________________。滤渣1的成分是_________,盐酸溶解MnCO3的离子方程式是_________________________________;
(2)用生石灰而不用NaOH调节pH的原因是_______________________________;
(3)滤液2中加入某种物质X可以除去Cu2+,最适合的是_______________;
A.MnO2 B.NaOH C.MnS
该反应的离子方程式是____________________________;
(4)将MnCl2转化为MnO2的一种方法是将酸化的NaClO3溶液氧化Mn2+,请补充并配平下列方程;____Mn2++_____ClO3-+______=____Cl2↑+____MnO2+_________;_________________
(5)将MnCl2转化为MnO2的另一种方法是电解法。(填“正极”或“负极”或“阴极”或“阳极”)
① MnO2在电解池的__________________(填“正极”或“负极”或“阴极”或“阳极”)生成;
② 若直接电解MnCl2溶液,生成MnO2的同时会产生少量Cl2。检验Cl2的操作是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废气中的NO2、CO2对环境具有极大影响,利用化学反应原理对其处理,对构建“绿水青山”生态文明有重要意义。请回答下列问题:
(1)下列说法正确的是_________
A.CO2和NO2与水反应所得溶液均为弱酸
B.NO2在一定条件下能与NH3反应生成环境友好的物质
C.通过测定溶液的pH,一定能判断H2CO3和HNO2的酸性强弱
D.Na2CO3溶液中加入硫酸可生成CO2
(2)H2在催化剂存在下能与NO2反应生成水蒸气和氮气而消去工业尾气中NO2的污染,
已知:①N(g)+2O2(g)=2NO2(g)ΔH=+133kJ/mol;②H2O(g)=H2O(1)ΔH=-44kJ/mol;③H2的燃烧热为285.8kJ/mol,该反应的热化学方程式为___________.
(3)CO2可在一定条件下转化为CH3OH。己知向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂和T1温度下,发生反应:CO2(g)+3H2(g) ![]() CH3OH(1)+H2O(1)ΔH<O,10min时达到平衡状态,10min后改变温度为T2,生成物全部为气体,20min时达到平衡状态,反应过程中部分数据见表:
CH3OH(1)+H2O(1)ΔH<O,10min时达到平衡状态,10min后改变温度为T2,生成物全部为气体,20min时达到平衡状态,反应过程中部分数据见表:
反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
0min | 2 | 6 | 0 | 0 |
10min | 4.5 | |||
20min | 1 |
①前10min内的平均反应速率v(CO2)=_______,20min时H2的转化率为_______。
②在其他条件不变的情况下,若30min时只改变温度为T3,达平衡时H2的物质的量为3.2mol,则T2______T3(填“>”“<”或“=”),在温度T2时,反应的化学平衡常数为______。
③在T1温度下,将容器容积缩小一倍,反应达平衡时CH3OH物质的量为____mol.和改变下列条件,能使H2的反应速率和转化率都一定增大的是____(填标号)。
A.在容积不变下升高温度
B.其它条件下不变,增加压强
C.在容积和温度不变下充入N2
D.在容积和温度不变下及时分离出CH3OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确且能达到相应实验目的的是
选项 | 实验目的 | 实验操作 |
A | 配制FeCl3溶液 | 将FeCl3固体溶解于适量蒸馏水 |
B | 称取2.0gNaOH 固体 | 先在托盘上各放一张滤纸,然后在右盘上添加2g 砝码,左盘上添加NaOH 固体 |
C | 检验溶液中是否含有NH4+ | 取少最试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
D | 验证铁的吸氧腐蚀 | 将铁钉放入试管中,用盐酸浸没 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质: A.O2 和 O3
B. ![]() O 和
O 和 ![]() O
O
C.CH3﹣CH2﹣CH2﹣CH3和CH3﹣CH(CH3)CH3
D.三氯甲烷和氯仿
E.甲烷和庚烷
F.异丁烷和 2﹣甲基丙烷
(1)组互为同位素;
(2)组两物质互为同素异形体;
(3)组两物质属于同系物;
(4)组两物质互为同分异构体;
(5)组是同一物质.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示方法正确的是( )
A.等量的硫蒸气和硫固体在氧气中分别完全燃烧,放出热量一样多
B.需要加热才能发生的反应一定是吸热反应
C.在101kpa时,2gH2完全燃烧,生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=﹣285.8kJ/mol
D.在强酸强碱稀溶液中:H+(aq)+OH﹣(aq)=H2O(l)△H=﹣57.3kJ/mol,若将含1molNaOH的溶液和含0.5molH2SO4的浓硫酸混合,放出的热量大于57.3 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应平衡常数K= ![]() .恒容条件下达到平衡时,温度升高H2浓度减小.下列说法正确的是( )
.恒容条件下达到平衡时,温度升高H2浓度减小.下列说法正确的是( )
A.该反应的化学方程式为CO+H2O ![]() CO2+H2
CO2+H2
B.该反应的焓变为正值
C.恒温恒容下,增大压强,H2浓度一定减小
D.升高温度,平衡右移,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铀(U)是一种稀有金属,制造氢弹的重要原料。提取铀涉及的反应为:UF4+ 2Mg![]() U + 2MgF2。在该反应中,作为还原剂的物质是______,被还原的物质是______;若反应中消耗1 mol Mg,则生成U______mol。
U + 2MgF2。在该反应中,作为还原剂的物质是______,被还原的物质是______;若反应中消耗1 mol Mg,则生成U______mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com