
【题目】已知NA是阿伏加德罗常数的值,下列说法正确的是( )
A.22.4L甲烷分子所含质子数为10NA
B.标准状况下,22.4L二氯甲烷的分子数约为NA个
C.1mol苯分子中含有的碳碳单键数为6NA
D.常温常压下,28.0g乙烯和丁烯的混合气体中含有的碳原子数目为2NA
科目:高中化学 来源: 题型:
【题目】298K时,向 ![]() 二元弱酸
二元弱酸 ![]() 溶液中滴加
溶液中滴加 ![]() 溶液,溶液中的
溶液,溶液中的 ![]() ,
,![]() ,
, ![]() 的物质的量分数
的物质的量分数![]()
![]() 随 pH的变化如图所示。下列说法错误的是
随 pH的变化如图所示。下列说法错误的是![]()
![]()

![]() 已知
已知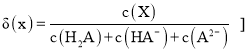
A.加入 ![]() 时,
时,![]()
B.当 ![]() ,
, ![]()
C.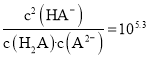
D.当混合溶液呈中性时,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水钴矿中除SiO2外,还有9.24%CoO、2.78%Fe2O3、0.96%MgO、0.084%CaO。从中提取钴的主要工艺流程如下:

(1)浸出过程中,CoO溶解的离子反应方程式为___,矿渣的主要成分是___、___。
(2)请配平下列除铁的化学方程式:
_Fe2(SO4)3+_H2O+_Na2CO3=_Na2Fe6(SO4)4(OH)12↓+_Na2SO4+_CO2↑
(3)除钙、镁过程中,逐渐加入NaF溶液,当CaF2开始沉淀时,溶液中![]() =___。[已知Ksp(CaF2)=1.0×10-10、Ksp(MgF2)=7.4×10-11]。
=___。[已知Ksp(CaF2)=1.0×10-10、Ksp(MgF2)=7.4×10-11]。
(4)“操作X”是___。进行该操作的主要目的是除去沉淀中的杂质离子,检验杂质中的主要阴离子是否除净的试剂是___。
(5)100t水钴矿最多可获得___tCoC2O44H2O产品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质溶液在电解质储罐和电池间不断循环.下列说法不正确的是

A.阳离子交换膜可阻止Br2与Zn直接发生反应
B.放电时正极的电极反应式为Br2+2e-=2Br-
C.充电时电极b连接电源的正极
D.放电时左侧电解质储罐中的离子总浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组学生用50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量计算中和热。下列说法正确的是( )

A.如图条件下实验过程中没有热量损失
B.图中实验装置缺少环形玻璃搅拌棒
C.烧杯间填满碎纸条的作用是固定小烧杯
D.若改用60mL0.50mol/L盐酸与50mL0.55mol/L的NaOH溶液进行反应,从理论上说所测反应热数值是相等的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是25 ℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是

A. 相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B. 碳酸钠溶液中滴加少量氯水的离子方程式H2O+2CO32-+Cl2===2HCO3-+Cl-+ClO-
C. 向0.1 mol·L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=9:5,此时溶液pH=5
D. 向浓度均为1×10-3mol·L-1的KCl和K2CrO4混合液中滴加1×10-3mol· L-1的AgNO3溶液,CrO42-先形成沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列装置完成系列实验,下列说法正确的是( )
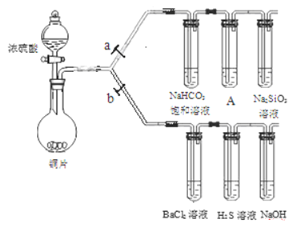
A. 铜和浓硝酸的反应与铜和浓硫酸的反应一样需要加热条件下才能进行
B. BaCl2溶液中会出现白色沉淀BaSO3
C. H2S溶液中会出现黄色沉淀,体现了SO2的还原性
D. 为验证碳、硅非金属性的相对强弱,A试管中的试剂可以是KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝镁合金是飞机制造、化工生产等行业的重要材料。研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其他元素)中镁的质量分数,设计了下列两种不同实验方案进行探究。填写下列空白:
(方案一)
(实验方案)将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。
实验中发生反应的化学方程式是_____________________________。
(实验步骤)
(1)称取10.8 g铝镁合金粉末样品,溶于体积为V物质的量浓度为4.0 mol·L-1NaOH溶液中,充分反应。则NaOH溶液的体积V≥_________mL。
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将________(填“偏高”、“偏低”或“无影响”)。
(方案二)
(实验方案)将铝镁合金与足量稀硫酸溶液反应,测定生成气体的体积。
(实验步骤)
(1)同学们拟选用下列实验装置完成实验:

你认为最简易的装置其连接顺序是A接(_____)( )接( )( )接( )(填接口字母,可不填满)。
(2)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小。于是他们设计了如图所示的实验装置。
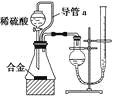
①装置中导管a的作用是_______________。
②实验前后量气管中液面读数分别为V1 mL、V2mL,则产生氢气的体积为___mL。
③若需确定产生氢气的量,还需测定的数据是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com